1. 서 론
2. 화학적 존재 형태 분석을 위한 해수 시료의 채수 방법
2.1 청정 해수 시료 채수법
2.2 용존 아연의 화학적 존재 형태 분석을 위한 해수 시료의 보관
3. 해수 시료의 전처리 및 분석법의 이론적 배경
3.1 해수 시료의 전처리 및 분석
3.2 용존 미량금속의 화학적 존재 형태 분석의 이론적 배경
4. 용존 아연의 화학적 존재 형태
4.1 용존 아연의 화학적 존재 형태에 대한 주요 연구 결과
4.2 식물 플랑크톤의 성장에 아연-유기착화합물이 미치는 영향
4.3 용존 유기배위자의 기원
5. 요 약
1. 서 론
해수 중에 존재하는 용존 금속 원소는 일반적으로 pM – nM (10-12 – 10-9 mol/L)의 농도로 존재하며, 이런 낮은 농도로 인하여 미량원소(Trace element) 또는 미량금속(Trace metal)으로 불리운다. 그 중 철(Fe), 구리(Cu), 니켈(Ni), 코발트(Co), 카드뮴(Cd), 아연(Zn) 등은 해양 환경에서 식물플랑크톤의 성장에 필수적인 미량영양염(micronutrient)으로서 궁극적으로는 해양의 탄소순환과 전지구적 기후변화에 영향을 미친다고 알려져 있다(Anderson, 2020).
하지만 초창기의 연구를 통해 보고된 용존 미량금속 농도는 같은 해역에서조차 매우 큰 차이를 보였는데, 당시 분석 기기의 검출 감도로는 매우 낮은 미량금속의 농도 레벨을 검출하기 어려운 것도 있었지만, 해수 시료의 채수 및 전처리, 분석 시에 사용되는 용기와 시약, 그리고 주변 환경으로부터 기인한 시료의 오염이 가장 큰 문제였다. 이후 분석 기술의 발전, 클린룸에 대한 개념의 도입과 함께 2000년대 들어 시작된 국제 연구 프로그램인 GEOTRACES를 통하여 미량금속의 오염을 최소화하는 청정 해수시료 채수법이 체계적으로 정립되었고(Cutter et al., 2013), 외양에서 미량금속의 농도가 매우 낮은 해수를 대량으로 채수, 미량금속 분석용 표준 해수(SAFe)를 전 세계에 배포하여 분석법의 검증을 도모한 결과 외양에서도 신뢰성이 높은 미량금속의 농도 자료를 생산할 수 있게 되었다(Johnson et al., 2007).
용존 미량금속 원소 중, 용존 아연(Zn)은 해양 환경에서 영양염형(Nutrient type)의 연직분포를 나타낸다(Fig. 1). 이는 표층에서 생물에 의해 용존 아연이 소비되고 유기 입자로 심층으로 이동하여 재광물화에 의해 다시 용존상으로 돌아오기 때문이다(Bruland and Lohan, 2006; Anderson 2020). 아연은 이산화탄소를 탄산염으로 변환시키는 효소인 Carbonic anhydrase (Morel et al., 1994; Lane and Morel, 2000), 유기인(Organic phosphate)을 무기인(Inorganic phosphate)으로 변환시키는 효소인 Alkaline phosphatase의 촉매로도 이용된다(Shaked et al., 2006).
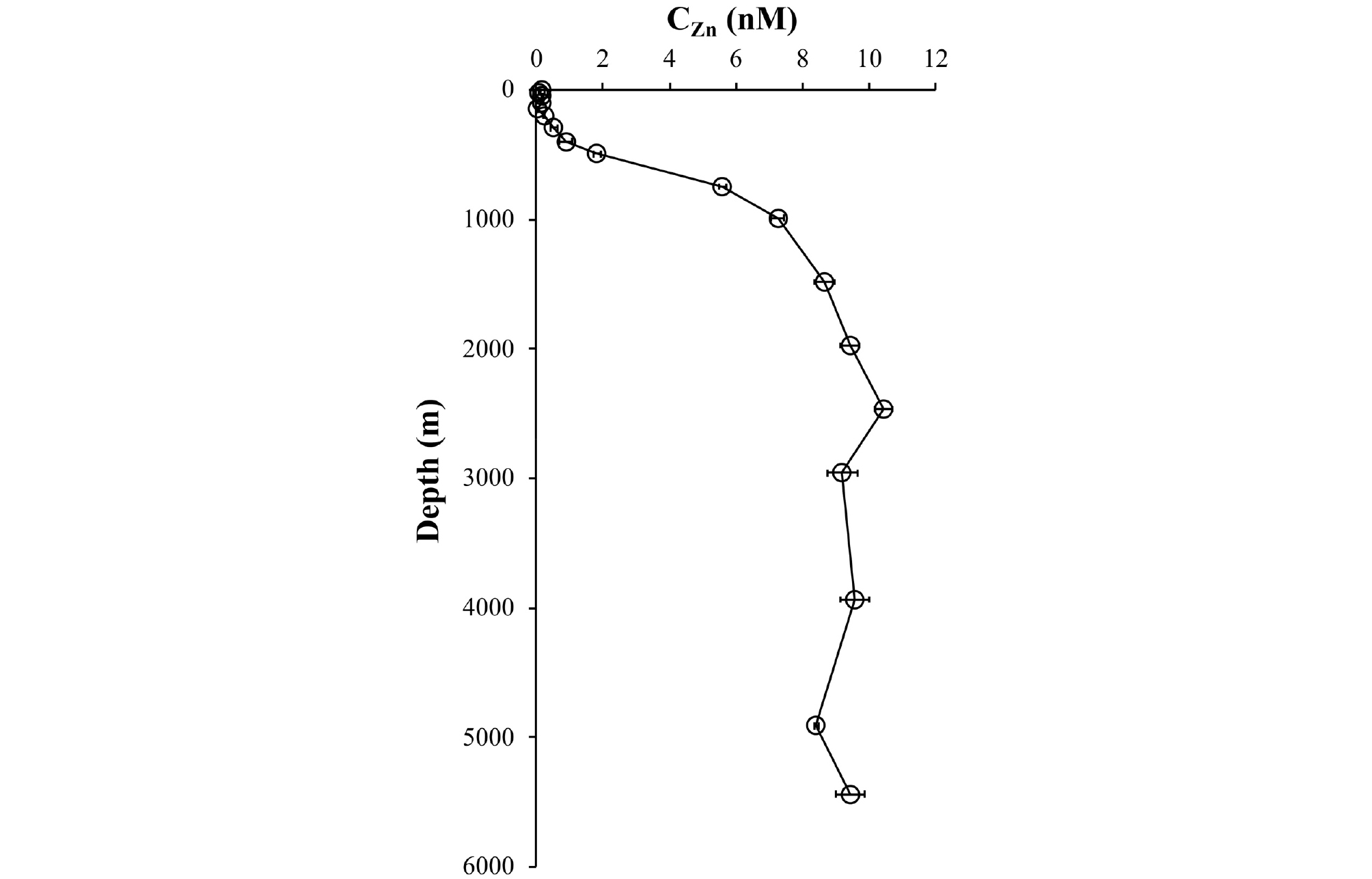
Fig. 1.
Vertical profile of total dissolved Zn (CZn) in the subtropical North Pacific (23° N, 160° E). Modified from Kim et al.(2015b).
해양 환경에 존재하는 용존 아연의 농도를 정확히 측정 할 수 있게 되었음에도 불구하고, 용존 아연의 생물가용성(bioavailability)을 정확히 평가하기는 어려운데, 가장 큰 원인으로서 용존 유기배위자(organic ligands)로 인한 아연의 화학적 존재 형태(chemical speciation)을 들 수 있다. 용존 유기배위자는 해양환경에서 용존 아연을 포함한 여러 용존 미량금속과 강하게 결합하여 금속-유기착화합물(organic complexed metals)을 형성하는 용존상(<0.2 µm)의 유기 분자(organic molecules)로 정의된다. 이 중 용존 아연과 결합하여 형성된 아연-유기착화합물(organic complexed Zn; ZnL)은 강한 결합력으로 인해 해리되기가 어렵고, 이로 인해 외양 표층에서는 식물플랑크톤의 성장과 밀접하게 연관되어 있는 아연 이온(Zn2+)이 총 용존 아연의 5% 이하로 감소하여 pM (10-12 M)의 농도 단위로 매우 낮게 존재하게 된다(Bruland, 1989). 따라서 용존 아연의 생물가용성을 이해하기 위해서는 농도 뿐만 아닌 화학적 존재 형태 또한 조사할 필요성이 대두되었으나, 농도 분석과 비교하여 복잡한 분석 과정과 분석 중 쉽게 오염이 일어날 수 있는 요인으로 인해 용존 아연의 화학적 존재 형태에 대한 실제 연구결과는 상대적으로 많이 보고 되어 있지 않다.
따라서 이 논문에서는 용존 아연의 화학적 존재 형태를 조사하기 위한 해수 시료의 획득, 분석 방법의 이론적 배경과 분석 방법에 대해 설명하고, 주요 연구 사례들을 소개하여 많은 연구자들이 용존 아연을 포함한 미량금속 원소의 농도 뿐만 아닌 화학적 존재 형태에 대해서도 관심을 가질 수 있는 기회를 제공하고자 하였다.
2. 화학적 존재 형태 분석을 위한 해수 시료의 채수 방법
2.1 청정 해수 시료 채수법
용존 미량금속의 농도 및 화학적 존재 형태 분석용 해수 시료 채취 시 오염이 일어날 수 있는 원인은 주변 모든 곳에 존재하는데, 그 예로 채수 장비를 장착하여 내리는 금속제 와이어로부터 유래한 오염, 연구선에 부착된 희생 전극(sacrificial anode)으로부터 유래한 오염, 시료의 분취 시 오염물질의 유입, 채수기의 산세척 미실시로 인해 채수기 자체로부터 유래하는 오염 등 있다(Cutter and Bruland, 2012; Kim et al., 2015a). 채수 중 일어날 수 있는 시료의 오염을 배재하기 위한 청정 해수시료 채수법은 여러 연구를 통하여 다양한 구성으로 확립되었다. 그 예로 채수기는 채취구를 닫히게 하는 스프링이 채수기 외부에 존재하는 Nisin-X type의 채수기 또는 테플론 코팅된 Go-Flo 채수기에 O-ring을 Viton제로 교체한 후 산세척을 실시하여 채수기에서 초래하는 금속 원소의 오염을 방지하고, 채수기를 장착하는 로젯 프레임은 에폭시 또는 폴리우레탄 코팅을 통해 프레임으로부터 유래할 수 있는 금속 오염을 배제하며, 선박과 로젯을 연결하는 케이블은 케블라, 티타늄, 또는 벡트란으로 피복된 케이블 등을 이용한다(Table 1). 그 외 네덜란드의 Royal Netherlands Institute for Sea Research (NIOZ)에서는 플루오르화 폴리비닐리덴(Polyvinylidene fluoride)제 채수기(PRINSTINE sampler)를 티타늄제 특수 프레임에 연결하고, 케블라로 피복된 케이블 사용하는 등의 독자적인 청정 해수시료 채수 시스템인 TITAN을 개발하였으며(de Baar et al., 2008; Rijkenberg et al., 2015), 현재 한국해양과학기술원에서도 동 시스템을 연구선 이사부에 도입하여 활발한 연구를 진행하고 있다(Kim et al., 2019). 청정 해수시료 채수법과 관련하여 보다 자세한 정보는 Kim et al.(2015a)와 Kim et al.(2019)을 참고하기 바란다.
Table 1.
Major components of trace-metal-clean sampling devices
| Sampler | Frame | Wire, Cable | Reference |
| Go-Flo water sampler | – | Kevlar wire | (Bruland et al., 1979) |
| Go-Flo water sampler | Epoxy painted Al frame | Kevlar cable | (Measures et al., 2008) |
| Go-Flo water sampler | Titanium Frame | Kevlar cable | (de Baar et al., 2008) |
| PRISTINE sampler | Titanium Frame | Kevlar cable | (Kim et al., 2019) |
| Go-Flo water sampler | Polyurethane coating Al frame | Vectran cable | (Cutter and Bruland, 2012) |
| External spring type water sampler (OTE) | Titanium frame | Plasma rope | (Wyatt et al., 2014) |
| External spring type water sampler (Niskin-X) | Polyurethane coating Al frame | Ti cable | (Kim et al., 2015a) |
| External spring type water sampler (Niskin-X) | Polyurethane coating Al frame | Vetran cable | (Obata et al., 2017) |
용존 미량금속 분석용 해수 시료는 청정 해수시료 채수법을 이용하여 채수를 실시한 다음, 외부 공기의 유입을 배제한 청정구역(clean container 또는 bubble)으로 채수기를 이동시킨 후, 채수기에 산세척을 실시한 캡슐필터(0.2 – 0.4 µm)를 직접 연결하여 해수 시료의 여과를 실시하게 되며, 이렇게 여과된 해수 시료는 산세척 한 low-density 또는 high-density 폴리에틸렌 용기에 담아 보관한다(Kim et al., 2015a).
2.2 용존 아연의 화학적 존재 형태 분석을 위한 해수 시료의 보관
일반적으로 용존 미량금속 농도 분석용 시료의 경우 금속 원소가 시료 보관 용기의 표면에 흡착되는 것을 배제하기 위해 시료에 초순도(ultra high purity) 염산 또는 질산을 첨가하여 < pH 1.8로 보관하지만(Cutter et al., 2013), 아연을 포함한 미량금속의 화학적 존재 형태 분석을 위한 해수 시료는 산을 첨가할 경우 유기배위자를 포함한 용존 유기물의 90% 이상이 분해되기 때문에 산을 첨가하여 시료를 보관하는 것은 불가능하다(Kim et al., 2015a). 그러므로 화학적 존재 형태 분석용 해수 시료는 시료에 존재하는 금속 원소가 용기에 흡착 되는 것을 최대한 방지하기 위하여 여과된 동일 해수 시료로 시료 용기를 충분히 헹구어 준 후 채취하며, 유기물이 분해되고 변화하는 것을 방지하기 위해 즉시 동결시켜 분석 전까지 냉동보관한다. 채취 후 냉동보관한 시료는 전처리 전에 미리 냉장보관하여 천천히 해동시킨 후 전처리를 진행한다.
3. 해수 시료의 전처리 및 분석법의 이론적 배경
3.1 해수 시료의 전처리 및 분석
해수 중 용존 아연의 화학적 존재 형태에 대한 분석은 배위자 교환 평형 / 흡착 농축 음극 벗김 전압전류법(Competitive Ligand Equilibrium / Adsorptive Cathodic Stripping Voltammetry; CLE-ACSV)법을 이용한다(van den Berg, 1985; Donat and Bruland, 1990). CLE-ACSV법은 전기화학 분석법의 하나로서 금속 이온의 농도에 비례해서 나타나는 환원 전류량을 측정하는 분석법이다. 이 논문에서는 아연의 화학적 존재 형태 분석을 위한 전처리 방법과 분석법의 이론적 배경을 설명하였다. 화학적 존재 형태를 알아보고자 하는 금속 원소에 따라 첨가해주는 인공 배위자가 다를 뿐 분석법의 이론적 배경은 동일하기 때문에 미량금속 원소 중 아연과 함께 상대적으로 화학적 존재 형태 연구가 활발히 이루어지고 있는 철과 구리의 분석법과 관련한 추가적인 정보는 Rue and Bruland(1995)와 Wong et al.(2018)을 참고하기 바란다.
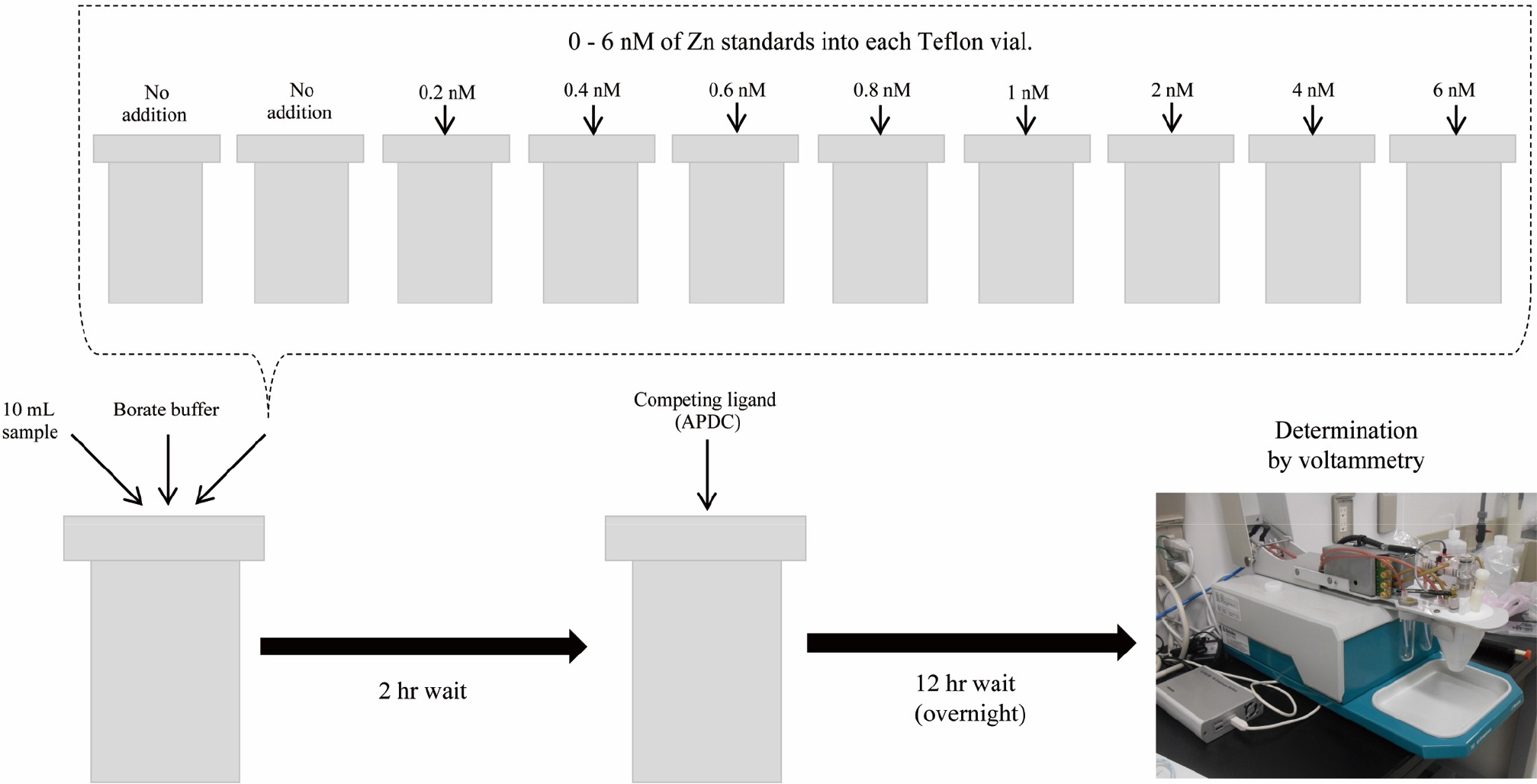
CLE-ACSV법을 이용한 아연의 화학적 존재 형태 분석을 위해 산세척을 실시한 테플론 바이알을 10개 정도 준비한다(Fig. 2). 측정하고자 하는 해수 시료에 존재하는 금속 원소가 테플론 바이알의 표면에 흡착되는 것을 방지하기 위하여 동일 해수 시료를 일정량 분취하여 각 테플론 바이알의 내부를 2-3회 신중히 헹구어 준 다음 사용된 해수 시료는 그대로 버린다. 이 후 각 테플론 바이알에 실제 측정을 위한 해수 시료를 10 mL씩 분취하고, pH를 8.2로 유지하기 위해 정제된 4 mM borate 버퍼를 첨가한다. 이 후 각각의 테플론 바이알에 점진적으로 증가하는 아연 표준물질의 농도(0–6 nM)를 첨가한 다음 화학 평형을 위하여 2시간 정도 대기한다. 마지막으로 각 테플론 바이알에 인공 배위자인 ammonium 1-pyrrolidinedithiocarbamate (APDC)를 첨가하여 시료에 존재하는 천연 유기배위자와 12시간 정도 경합 시킨다(Fig. 2).
이렇게 전처리에서 첨가된 아연 표준물질은 시료에 존재하는 천연 유기배위자와 우선적으로 결합하게 되고, 이렇게 형성된 아연 결합 유기착화합물은 전기화학적으로 비활성 상태가 되어 볼타메트리(Voltammetry)에서 아연의 환원 전류는 검출되지 않지만, 첨가된 아연 표준물질의 농도가 시료에 존재하는 천연 유기배위자의 농도보다 높을 경우 천연 유기배위자와 결합하고 남아 있는 아연은 이후 첨가해주는 APDC와 결합하여 전기화학적으로 측정이 가능한 Zn-PDC를 형성하게 된다.
전처리가 완료된 시료는 볼타메트리의 테플론 셀컵에 옮겨 분석을 실시한다(Fig. 2). 실제 분석을 시작하기에 앞서 시료에 질소 기체를 일정시간 주입하여 시료에 존재하는 산소를 모두 제거함으로서 산소에 의해 나타나는 노이즈 전류를 차단한다. 분석 시 Zn-PDC는 기준 전극인 Ag/AgCl에 대하여 –0.6 V의 전위가 가해진 수은 전극에 흡착, 농축되고, 수은 전극에 –0.75 V에서 -1.2 V로 음의 방향으로 전위를 주사하면 –1.0 V 가까이에서 Zn-PDC의 Zn2+가 Zn0로 환원되며, 이때 얻어지는 환원 전류량은 Zn-PDC의 농도에 비례해서 나타난다(Fig. 3a).
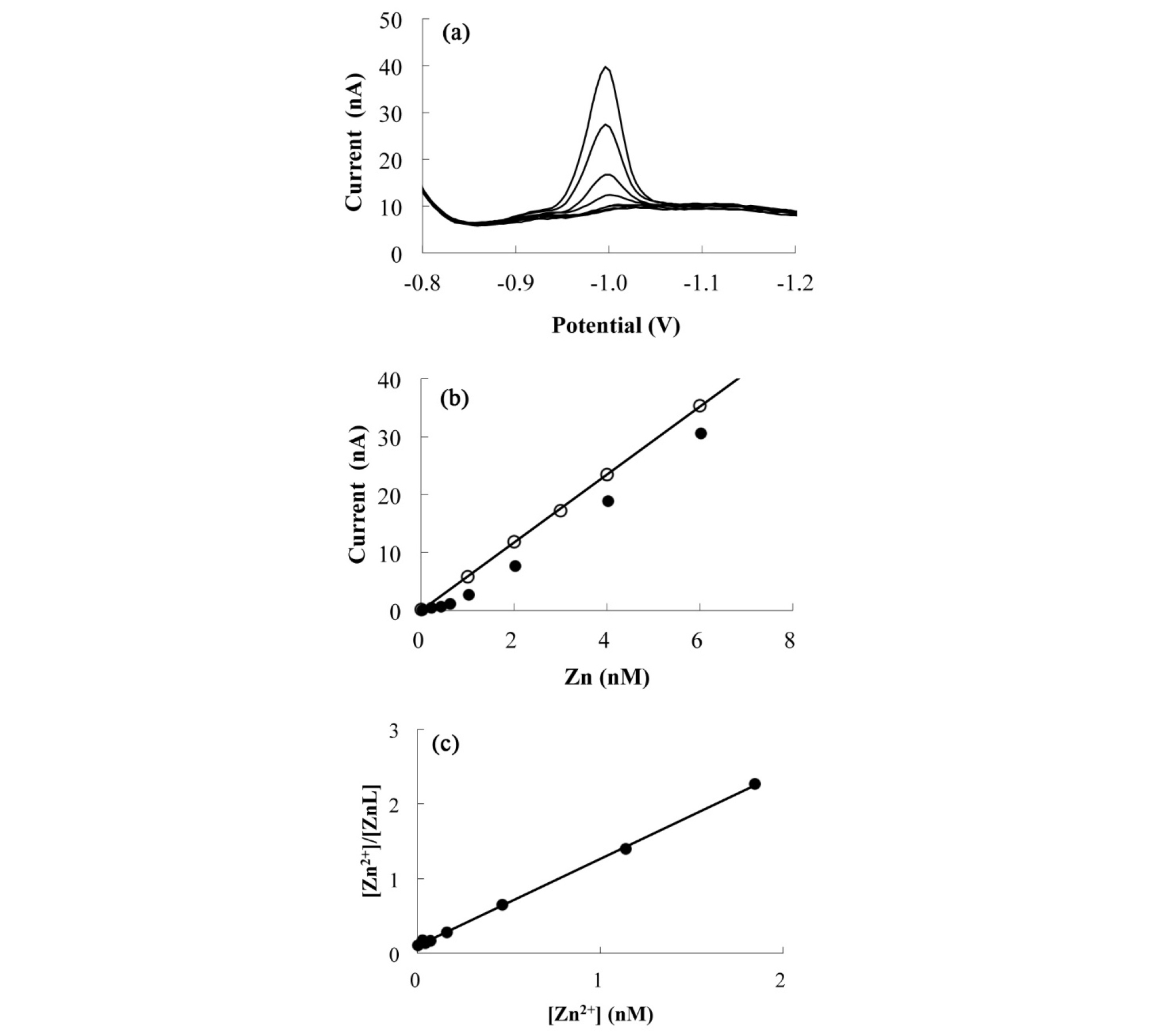
Fig. 3.
Example of Zn titration data. (a) Voltammetric scans for Zn additions. (b) The response of Zn peak current with increasing Zn additions. The line and blank circles indicate the response of UV-irradiated sample. (c) Linear relationship obtained by transforming the titration data. The calculated CL and log in this linear relationship were 0.9 nM and 10.1, respectively. Modified from Kim et al.(2015c).
3.2 용존 미량금속의 화학적 존재 형태 분석의 이론적 배경
이렇게 측정을 통해 얻어진 적정 곡선(titration curve)을 이용(Fig. 3b), 일련의 계산을 통해 해수 중에 존재하는 천연 유기배위자의 농도(CL), 용존 아연이 유기배위자와 얼마나 강하게 결합하여 존재하고 있는지를 나타내는 조건 안정도 상수(conditional stability constant; ), 해수 시료에 존재하는 아연 이온의 농도(Zn2+)를 산출할 수 있다. 해수 시료에 존재하는 아연의 총 농도(CZn)는 별도의 농도 분석을 통해 얻을 필요가 있으며, 다음과 같이 정의 된다.
| $${\mathrm C}_{\mathrm{Zn}}=\lbrack\mathrm{ZnL}\rbrack+\lbrack\mathrm{Zn}'\rbrack+\lbrack\mathrm{Zn}^{2+}\rbrack$$ | (1) |
여기서 [ZnL]는 천연 유기배위자와 결합한 아연-유기착화합물의 농도, [Zn']는 무기태 아연(inorganic Zn)의 농도, 그리고 [Zn2+]는 아연 이온의 농도를 나타낸다. 여기서 Zn'과 Zn2+은 불안정한 아연(labile Zn; Znlabile)으로 정의되는데, Znlabile은 APDC와 결합하여 Zn-PDC화합물을 형성, 볼타메트리를 통해 환원 전류의 측정이 가능한 아연을 의미하며, [Znlabile] = [Zn'] + [Zn2+]의 관계식을 가진다. 해수 시료에서 유기배위자와 결합하여 유기착화합물을 형성한 아연은 다음과 같이 정의 된다.
| $$\mathrm K'_{\mathrm{ZnL},\mathrm{Zn}^{2+}}=\frac{\lbrack\mathrm{ZnL}\rbrack}{\lbrack\mathrm{Zn}^{2+}\rbrack\lbrack\mathrm L'\rbrack}$$ | (2) |
여기서 는 [Zn2+]에 대한 아연-유기착화합물의 조건 안정도 상수를 나타내며, [L']는 해수 시료에 존재하는 천연 유기배위자 중 아연과 결합하지 않은 유기배위자(free ligand)의 농도를 나타낸다.
해수 시료에 존재하는 천연 유기배위자의 총 농도(CL)의 경우 다음과 같이 정의 된다.
| $${\mathrm C}_{\mathrm L}=\lbrack\mathrm{ZnL}\rbrack+\lbrack\mathrm L'\rbrack$$ | (3) |
식 (2)의 [L’]를 식 (3)으로 치환하여 정리하면 아래의 관계식으로 나타낼 수 있다.
여기서 x축을 [Zn2+], y축을 [Zn2+]/[ZnL]로 정리하여 그래프로 나타낼 경우, 선형관계에서의 기울기는 1/CL에 해당하며, y축의 절편은 에 해당하므로 CL과 을 구할 수 있게 되며, 이를 van den Berg/Ružić linearization라 한다(Ružić, 1982; van den Berg, 1982)(Fig. 3c). 식 (4)를 통해 van den Berg/Ružić linearization에 표시되는 x축의 [Zn2+]와 y축의 [Zn2+]/[ZnL]의 값은 해수 시료에 아연 표준물질의 농도를 점진적으로 증가시킨 후 볼타메트리 측정을 통해 얻어지는 각각의 환원 전류값(ip)을 이용해 얻어질 수 있다. 먼저 식 (4)의 [Zn2+]는 다음으로 정의 된다.
| $$\lbrack\mathrm{Zn}^{2+}\rbrack=\frac{i_P}{S\times\alpha'}$$ | (5) |
여기서 ip는 볼타메트리에 의해 검출되는 환원 전류값을 나타내며, S는 볼타메트리의 감도(전류값/아연농도)를 나타내는데, 이는 자외선을 조사(UV-irradiation)하여 천연 유기배위자를 모두 분해, 제거한 해수 시료에 표준물질을 첨가하여 볼타메트리로 얻어지는 검량선을 통해 구한다. 볼타메트리를 이용한 측정에서 ip/S 값은 위에서 언급한 바와 같이 [Znlabile] (= [Zn'] + [Zn2+])을 의미하기 때문에 볼타메트리에서 측정되는 환원 전류값에서 [Zn2+]을 계산하기 위해서는 아연의 부반응계수(side reaction coefficient; 를 넣어줄 필요가 있으며, 는 다음과 같이 정의 된다.
| $$\alpha'=\alpha_{\mathrm{Zn}}+\alpha_{\mathrm{ZnPDC}}$$ | (6) |
여기서 는 무기 아연의 부반응계수를 나타내며, pH 8.2의 해수에서는 이온페어링 모델에 의해 2.2의 값을 가진다(Turner et al., 1981). 는 Zn-PDC의 부반응계수로서 첨가한 APDC의 농도에 의해 결정 되며, 다음과 같이 정의 된다.
| $$\alpha_{\mathrm{ZnPDC}}=\mathrm K'_{\mathrm{ZnPDC}}\lbrack\mathrm{APDC}'\rbrack$$ | (7) |
여기서 는 조건 안정도 상수이며 [APDC’]는 아연 이온과 결합하지 않은 APDC의 농도를 의미한다. 하지만 통상 해수 시료에 첨가하는 APDC의 농도(25 – 50 µM)는 아연의 농도보다 월등히 높기 때문에 [APDC’]를 대신하여 첨가한 APDC의 총 농도 값(=[ADPC])을 이용한다. 값은 pH 8.2의 해수에서 104.4로 보고되어 있다(van den Berg, 1985).
식 (4)를 통해 van den Berg/Ružić linearization에 표시되는 y축의 [Zn2+]/[ZnL]에서 [ZnL]는 다음으로 계산될 수 있다.
| $$\lbrack\mathrm{ZnL}\rbrack={\mathrm C}_{\mathrm{Zn}}-\left(\frac{i_p}s\right)$$ | (8) |
위에서 언급한 바와 같이 (ip/S)는 [Znlabile]을 의미하기 때문에 식 (1)을 근거로 [ZnL]이 계산된다. 식 (5)와 식 (8)을 정리하면 [Zn2+]/[ZnL]는 다음과 같이 나타낼 수 있다.
| $$\frac{\lbrack\mathrm{Zn}^{2+}\rbrack}{\lbrack\mathrm{ZnL}\rbrack}=\frac{i_p}{\alpha'\times((S\times C_{\mathrm{Zn}})-i_p)}.$$ | (9) |
즉, 식 (5)와 식 (9)를 이용하여 식 (4)의 van den Berg/Ružić linearization의 도식화가 가능해지고, 이를 통해 CL와 를 구할 수 있게 된다. 마지막으로 해수 시료에 존재하는 실제 [Zn2+]는 다음의 이차방정식을 이용하여 구할 수 있다(Ellwood and van den Berg, 2000).
4. 용존 아연의 화학적 존재 형태
4.1 용존 아연의 화학적 존재 형태에 대한 주요 연구 결과
Table 2는 용존 아연의 화학적 존재 형태에 대한 주요 연구 결과를 정리한 것이다. 대부분의 해역에서 아연과 결합하는 용존 유기배위자의 농도(CL)은 nM (10-9 M)의 농도 단위로 존재한다. 해역별로 비교 할 경우 대부분의 외양역(open ocean)에서는 연안역(marginal sea)에 비해 상대적으로 낮은 용존 유기배위자의 농도와 높은 조건 안정도 상수를 가지는 것을 보여준다. 외양역은 거리상으로 육지와 멀리 떨어져 있기 때문에 육상기원 유기배위자의 유입 가능성이 높은 연안역과 비교하여 상대적으로 낮은 용존 유기배위자의 농도를 보이는 것으로 알려져 있다(Kim et al., 2015b). 유기배위자의 기원에 대해서는 아래에서 자세히 소개하고자 한다. 용존 아연이 유기배위자와 얼마나 강하게 결합하여 존재하고 있는지를 나타내는 조건 안정도 상수는 연안역에서 상대적으로 낮게 나타나는 것으로 보고 되었는데(Table 2), 육상기원 유기배위자가 상대적으로 약한 결합력을 가지고 있을 가능성을 시사하나, 외양역과 연안역에 존재하는 유기배위자의 분자구조에 대한 정보가 전무하기 때문에 아직까지도 연안역에서 상대적으로 낮게 나타나는 조건 안정도 상수가 어떤 원인에 의해 나타나는지에 대해서는 잘 알려지지 않았다(Bruland and Lohan, 2006; Kim et al., 2015b).
Table 2.
Zn chemical speciation data from relevant studies
| Region | Sample | [CL] | Reference | ||
| (nmol/L) | |||||
| Open Ocean | Central subtropical North Pacific | Profile | 1.0-1.5 | 10.7-11.3 | (Bruland, 1989) |
| Eastern North Pacific | 60 and 150 m | 1.7-2.3 | 11.0-11.5 | (Donat and Bruland, 1990) | |
| Eastern subarctic North Pacific | 15 m | 0.7 | 10.5 | (Lohan et al., 2005) | |
| 15-150 m | 1.1-2.6 | 10.3-11.3 | (Jakuba et al., 2012) | ||
| Western subarctic North Pacific | 25-40 m | 2.3-2.7 | 10.1-10.8 | (Jakuba et al., 2012) | |
| South Pacific | 20 m | 1.3 | 10.2 | (Ellwood, 2004) | |
| 20 m | 1.2 | 10.6 | (Ellwood, 2004) | ||
| Western subtropical North Pacific | 6-198 m | 0.2-0.5 | 9.5-10.8 | (Kim et al., 2015b) | |
| Western subarctic North Pacific | 10-37 m | 0.7-1.2 | 9.7-10.2 | (Kim et al., 2015b) | |
| Northeastern Indian Ocean | 17 m | 0.5 | 10.0 | (Kim et al., 2015c) | |
| Northeastern Atlantic | Surface | 0.4-2.5 | 10.0-10.5 | (Ellwood and van den Berg, 2000) | |
| Central North Atlantic | Profile | 0.9-1.5 | 9.8-10.5 | (Jakuba et al., 2008) | |
| Profile | 0.6-1.3 | 9.8-11.3 | (Jakuba et al., 2008) | ||
| Southern Ocean | 10-200 m | 1.4-5.3 | 9.1-10.4 | (Baars and Croot, 2011) | |
| Marginal Sea | Sea of Okhotsk | 20 m | 2.6 | 9.5 | (Kim et al., 2015b) |
| East Sea | 20 m | 1.3 | 9.2 | (Kim et al., 2015b) | |
| Andaman Sea | 5-100 m | 0.4-0.9 | 9.6-11.4 | (Kim et al., 2015c) | |
| Bering Sea | 20 m | 3.6 | 9.6 | (Jakuba et al., 2012) | |
| Black Sea | 10 m | 7.8-16.6 | 9.7-10.7 | (Muller et al., 2001) | |
Fig. 4는 아열대 북태평양에서 얻어진 용존 아연의 화학적 존재 형태에 대한 연직 분포를 보여준다. 표층에서 용존 유기배위자의 농도([CL])는 아연의 총 농도([CZn])와 비교하여 상대적으로 높게 나타나는 것을 알 수 있으며(Fig. 4a), 용존 유기배위자가 아연과 결합하여 아연-유기착화합물(ZnL)을 형성하게 되고, 이로 인하여 아연 이온(Zn2+)은 pM (10-12 M)의 낮은 농도로 나타나는 것을 알 수 있다(Fig. 4b). 상대적으로 용존 아연의 총 농도가 낮은 아열대 북태평양, 아열대 대서양, 인도양의 표층에서는 95% 이상의 아연의 아연-유기착화합물로 존재한다고 알려져 있으나(Bruland, 1989; Donat and Bruland, 1990; Ellwood and van den Berg, 2000; Jakuba et al., 2012; Kim et al., 2015b; Kim et al., 2015c), 반대로 아한대 북태평양, 남극해와 같이 용존 아연의 표층 농도가 상대적으로 높게 나타나는 해역에서는 종종 아연의 총 농도가 유기배위자의 농도보다 높기때문에 일부 아연은 유기배위자와 결합하지 못한 형태로 존재하게 되고, 이로 인해 아연 이온의 농도가 상대적으로 높게 나타나는 것으로 보고되었으며(Baars and Croot, 2011; Kim et al., 2015b), 연안역의 경우 주변 환경 요인에 인한 용존 아연 또는 용존 유기배위자의 유입으로 아연 이온의 농도는 매우 다양하게 나타날 수 있다(Muller et al., 2001; Jakuba et al., 2012; Kim et al., 2015b).
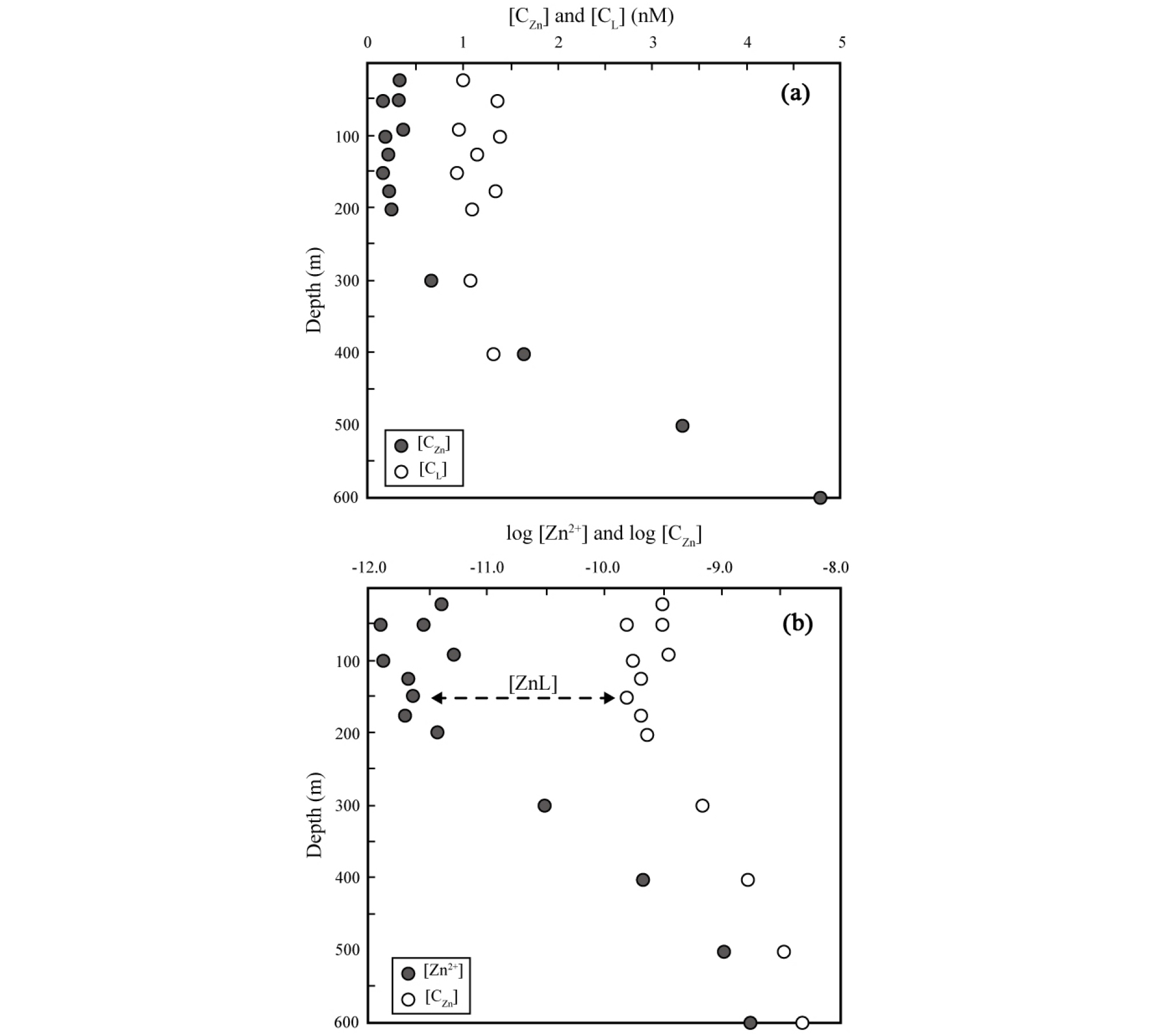
Fig. 4.
Concentration profiles of (a) total dissolved Zn ([CZn]), and total organic ligands ([CL]) and (b) free Zn ion ([Zn2+]) and total dissolved Zn ([CZn]) in the upper 600 m of the subtropical North Pacific (28° N, 158° W). Note that [ZnL] between [Zn2+] and [CZn] indicate the concentration of organic complexed Zn. Modified from Bruland(1989).
4.2 식물 플랑크톤의 성장에 아연-유기착화합물이 미치는 영향
아연-유기착화합물이 식물플랑크톤의 성장에 미치는 영향에 대해 설명하기 앞서, 미량금속 원소 중 용존 구리에 대하여 간략히 설명하고자 한다. 본래 해양환경에서 용존 구리의 총 농도는 10-10 – 10-9 M의 농도 범위를 가진다. 해당 농도 범위에서 구리는 식물플랑크톤에 독성으로 작용하게 되는데, 즉 용존 구리가 유기착화합물과 결합한 형태가 아닌, 구리 이온으로 전부 존재할 경우 해당 환경에서 구리는 식물 플랑크톤의 성장을 저해한다(Brand et al., 1986). 다행히 용존 구리는 유기배위자와 강하게 결합하여 구리-유기착화합물을 형성하게 되고, 이로 인해 식물플랑크톤의 성장에 직접적으로 이용되는 구리 이온(Cu2+)의 농도를 10-13 M까지 낮추게 되며 비로소 구리는 해당 농도에서 식물플랑크톤의 성장을 저해하는 독성 원소가 아닌 필수 미량영양염으로 이용될 수 있게 된다(Brand et al., 1986; Moffett and Brand, 1996).
해양환경에 존재하는 용존 아연의 총 농도 또한 10-10 – 10-9 M의 범위를 가지지만, 용존 구리와 다르게 이 농도 범위에서 아연은 식물플랑크톤에 독성으로 작용하지 않는다. 오히려 아연-유기착화합물의 형성으로 인해 pM단위의 농도로 낮아진 아연 이온은 특정 식물플랑크톤의 성장을 제한시키는 원인이 될 수 있다고 제안 되었다(Sunda and Huntsman, 1992). Fig. 5는 아연 이온 첨가에 따른 여러 식물플랑크톤의 비성장속도(Specific growth rate)의 결과를 보여주는데, 연안종인 Thalassiosira pseudonana와 Thalassiosira weissflogii는 아연 이온 농도 10-11 M 이하에서 성장이 제한되어 있는 것을 알 수 있으며, 아연 이온 농도가 10-11 M 이상으로 증가할 경우 일정한 성장 속도를 보였다. 하지만 10-7 M의 아연 이온 농도에서 Thalassiosira weissflogii의 성장 속도는 급격히 감소하였는데, 비록 해당 농도는 해양 환경에서 보고되는 농도보다도 월등히 높지만, 만약 모든 용존 아연이 이온 형태로 존재한다면, 해당 농도 범위에서는 아연이 독성으로 작용할 수 있다는 것을 의미한다. 반면, 외양종인 Thalassiosira oceanica와 Emiliania huxleyi의 경우 낮은 아연 이온 농도(10-12.3 M)에서도 제한 없이 성장하는 것으로 나타났는데 외양은 연안과 비교하여 아연의 농도가 매우 낮기 때문에 해당 종들의 경우 매우 낮은 농도의 아연만으로도 성장이 가능하도록 발달한 것으로 해석된다(Sunda and Huntsman, 1992).
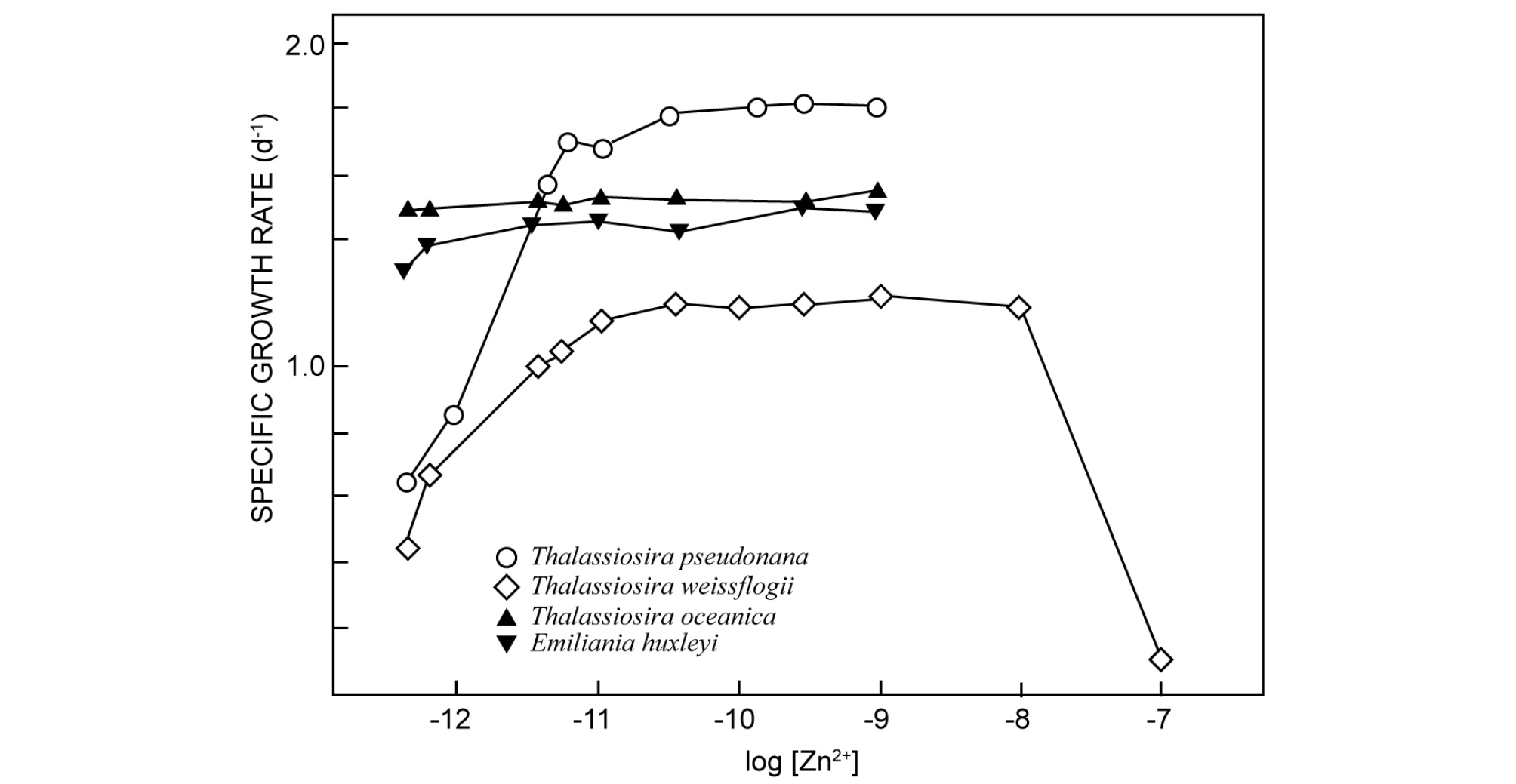
Fig. 5.
Specific growth rate as functions of Zn2+. Blank symbols indicate coastal phytoplankton species, whereas filled symbols were oceanic. All phytoplankton species were Diatoms except for Emiliania Huxley, which was coccolithophores. Modified from Sunda and Huntsman(1992).
이렇게 대부분의 용존 아연이 아연-유기착화합물 형태로 존재하게 됨으로써 특정 식물플랑크톤의 성장을 제한할 가능성이 커지지만, 반대로 용존 아연의 체류시간은 증가하게 된다. 일반적으로 금속 이온은 입자에 흡착되어 표층에서 제거되기 쉽다. 반면에 아연이 유기배위자와 결합하여 형성된 아연-유기착화합물은 아연의 입자반응성을 감소시켜 입자 침강(Scavenging)으로 인한 아연의 제거율을 낮추며, 이로 인해 아연이 용존상에 계속 남아 있을 수 있게 한다. 이렇게 용존상에 남아 있는 아연을 식물플랑크톤이 사용한다는 “스마트 뱅킹”이라는 가설 또한 제안되었으나(Bruland, 1989), 아직까지도 강하게 결합되어 있는 아연-유기착화합물이 어떠한 과정을 통해 식물플랑크톤에 흡수될 수 있는지에 대해서는 잘 알려지지 않았다.
4.3 용존 유기배위자의 기원
아연과 결합하여 아연-유기착화합물을 형성하는 용존 유기배위자의 기원으로는 휴믹산(Campbell et al., 2002), 하구역 퇴적물의 공극수로부터 유래한 용존 유기물(Skrabal et al., 2006), 식물플랑크톤 또는 박테리아로부터 유래한 용존 유기물질(Bruland, 1989) 등이 거론되고 있으나, 위에서 언급한 바와 같이 용존 유기배위자의 분자구조에 대한 정보가 전무하기 때문에 용존 유기배위자의 생성 과정과 기원은 앞으로 밝혀야 할 숙제이다.
Kim et al.(2015b)는 외양역인 아열대, 아한대 북태평양과 연안역인 오호츠크해, 동해에서 얻어진 유기배위자의 농도와 Chl a간의 상관관계를 비교한 결과 해역별로 다른 특성을 보이는 것을 확인하였으며, 이를 통해 유기배위자의 주된 기원은 해역별로 상이하다고 제안하였다(Fig. 6). 해역별로 얻어진 Chl a와 유기배위자 농도 간 상관관계를 보면 (1) 아열대 북태평양에서는 Chl a와 유기배위자의 농도 모두 상대적으로 낮게 나타났으며, (2) 아한대 북태평양에서는 Chl a와 유기배위자의 농도 모두 상대적으로 높게 나타났고, (3) 연안역(오호츠크해, 동해)에서는 낮은 Chl a가 나타났음에도 유기배위자의 농도는 높게 나타났다(Fig. 6).
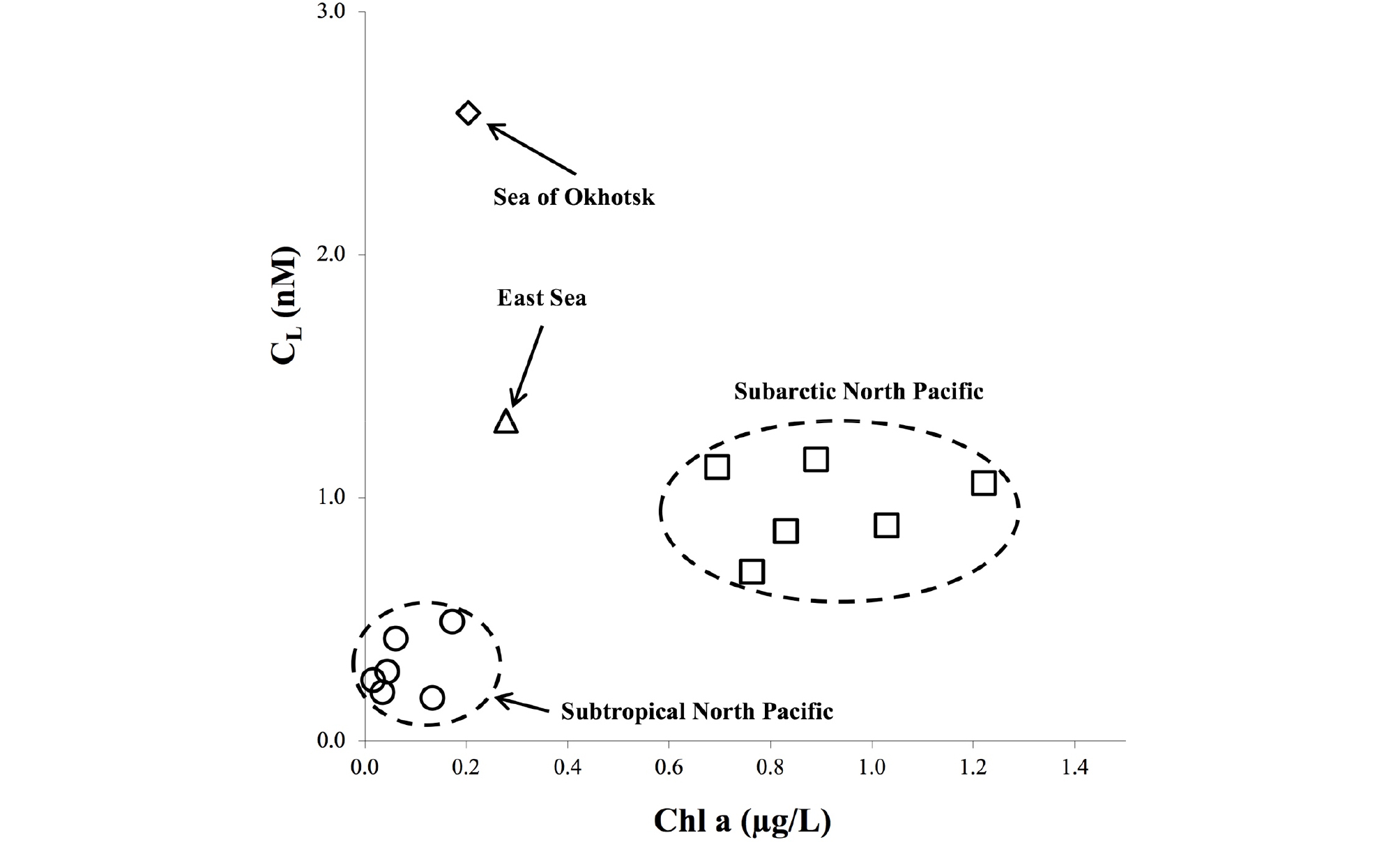
Fig. 6.
Comparison of Chl a and total organic ligand concentrations ([CL]) in the subtropical North Pacific (23° N, 160° E; circles), subarctic North Pacific (47° N, 160° E; 47° N, 180°; squares), Okhotsk Sea (45°15′ N, 160°04′ E; diamond), and East Sea (42°43′ N, 138°13′ E; triangle). Modified from Kim et al.(2015b).
Bruland(1989)는 상대적으로 육상기원 물질유입의 영향이 적은 외양역에서의 경우 식물플랑크톤 또는 박테리아로부터 유래한 용존 유기물질이 주된 유기배위자의 기원일 것이라고 제안하였다. 아열대, 아한대를 포함한 북태평양에서 유기배위자의 농도는 Chl a와 양의 상관관계(R2 = 0.81)를 나타내었는데(Fig. 6), 이는 외양역에 존재하는 유기배위자가 현장 표층에 존재하는 식물플랑크톤 또는 박테리아로부터 유래한다는 것을 뒷받침한다.
Jakuba et al.(2012)는 베링해에서 상대적으로 높은 Chl a (0.86 μg/L)와 유기배위자의 농도(3.6 nM)를 보고하였고, 이 결과를 토대로 외양역뿐만 아닌 연안역에서도 식물플랑크톤 또는 박테리아가 유기배위자의 주된 기원일 가능성을 제안하였다. 하지만, 오호츠크해와 동해에서는 낮은 Chl a가 나타났음에도 유기배위자의 농도는 상대적으로 높게 나타났으며, 해당 해역에서 얻어진 결과들은 북태평양 외양역에서 얻어진 상관관계에서 벗어나 있는 것을 알 수 있다(Fig. 6), 이 결과는 다른 기원의 용존 유기배위자가 해당 해역에 존재할 가능성을 시사한다. 낮은 표층 염분 값을 보인 오호츠크해의 경우 아무르강 하천수의 유입을 통해 많은 양의 휴믹산이 오호츠크해로 유입된다고 보고되었으며(Nakatsuka et al., 2004), 이로 인해 오호츠크해에 존재하는 용존 유기배위자는 휴믹산이 주된 기원일 가능성이 제시되었다(Kim et al., 2015b). 동해 표층 또한 Chl a와 비교하여 상대적으로 높은 용존 유기배위자의 농도가 얻어졌는데(Fig. 6), 이는 동해의 표층 순환에 큰 영향을 끼치는 대마난류를 통한 용존 유기배위자의 유입이 주된 기원으로서 제안되었다(Guo et al., 2006). 이와 같이 해역별로 용존 유기배위자의 기원은 환경에 따라 다양하게 나타날 가능성이 높으며, 용존 유기배위자의 새로운 기원과 유기배위자의 순환 과정 등 보다 자세한 정보는 향후 다양한 연구를 통하여 밝혀질 것이라 예상된다.
5. 요 약
이상에서 화학적 존재 형태에 대한 개념과 측정 방법, 해양 환경에서 아연과 결합하여 유기착화합물을 형성하는 용존 유기배위자의 역할과 기원에 대하여 간단히 소개하고, 관련한 연구의 예들을 살펴보았다. 볼타메트리를 이용한 CLE-ACSV 분석법을 통하여 미량금속의 화학적 존재 형태에 대한 분석이 가능해지고, 그 결과로서 용존 금속과 결합하여 금속-유기착화합물을 형성하는 유기배위자의 농도, 금속 이온의 농도, 조건 안정도 상수 등 미량금속의 농도 뿐만 아닌 보다 다양한 화학적 존재 형태에 대한 자료의 축적이 가능하게 되었다. 하지만 미량금속의 분석은 오염의 위험성이 매우 높고, 특히 화학적 존재 형태에 대한 분석의 경우 분석 과정이 복잡하기 때문에 상대적으로 적은 연구 결과가 보고되어 있으며, 한반도 주변 해역에서는 아직 연구가 본격적으로 이루어지지 않고 있다. 앞으로 국내 연구자들이 꾸준한 관심을 가지고 한반도 주변 해역을 포함한 여러 해역에서 용존 미량금속의 농도 뿐만 아닌 화학적 존재 형태에 대한 연구를 진행할수록 보다 자세한 미량금속의 생지화학적 순환과정이 밝혀질 것으로 기대된다.