1. 서 론
2. 자료 및 방법
3. 결과 및 토의
3.1 표층 수온, 염분, 탄산계 매개변수, 탄산이온의 분포
3.2 완충인자들의 표층 분포
3.3 수온, 염분과 완충역량의 관계
3.4 수괴별 완충역량
4. 요 약
1. 서 론
해양은 인류가 배출한 이산화탄소(CO2)의 약 25%를 흡수하여 실제 대기에 누적되는 양을 배출량의 절반 가량으로 줄이는 데 기여하는 거대한 탄소 저장고이다(Sabine et al., 2004; Gruber et al., 2019; Friedlingstein et al., 2020). 이러한 해양의 역할은 지구온난화를 완화시키는 데 결정적으로 기여해왔지만 해양이 흡수한 CO2는 수소이온(H+)을 방출하여 해양산성화를 일으킨다(Gattuso and Hansson, 2011). 다행히도 해수는 산성화에 저항하는 자체적인 능력이 있으며 이를 완충역량(buffer capacity)이라고 한다. 해수가 CO2를 완충하는 과정은 아래 식 (1)로 요약된다:
탄산이온()은 해수로 하여금 완충능력을 가지도록 하는 주 화학종으로 H+뿐만 아니라 CO2도 함께 중화하여 해양이 인류기원 CO2를 흡수하는 효율에도 관여한다. 해수의 약알칼리성(표층 해수의 pH~8.1) 특성을 주도하는 탄산이온이 소모된 결과로 현재 해양에서는 지질역사에서 아주 빠르게 산성화가 진행되고 있다(Rubey, 1951; Broecker and Clark, 2001; Caldeira and Wickett, 2003; Feely et al., 2004; Orr et al., 2005; Gattuso and Hansson, 2011).
해양산성화는 추가적인 해양의 이산화탄소 흡수, 탄산 광물의 침전과 용해, 해양 생물의 기능과 생존에 영향을 미치므로 해양의 완충을 이해하고 정량화하는 것이 중요하다(Middelburg et al., 2020). 완충역량을 정량화 하는 방법 중 가장 널리 쓰이는 Revelle 인자(Revelle factor=𝜕In[CO2]/𝜕InDIC; Revelle and Suess, 1957)는 사실상 입력량(DIC)의 변화에 대한 산출량([CO2])의 변화율을 나타내는 민감도(sensitivity) 계수이다(Middelburg et al., 2020). 본 연구에서는 이러한 혼란을 피하기 위해 Egleston et al.(2010)이 제시한 완충인자를 사용하였다(Table 1). 여섯 가지 모두 민감도 계수의 역수로서 완충역량을 나타내며, moles L-1(또는 moles kg-1)라는 단위를 가져 단순한 예측 또는 역추정이 가능하다. 또한 DIC 또는 TA가 변할 때 [CO2], [H+](또는 pH), (또는 [])가 변화에 저항하는 능력을 각각 정량화 할 수 있다. 가 DIC 또는 TA가 변할 때 (=[Ca2+][]/Ksp)의 저항뿐만 아니라 []의 저항을 나타내기도 하는 이유는 DIC나 TA가 변할 때 [Ca2+]와 Ksp는 변하지 않기 때문이다.
주변해(marginal sea)는 전체 해양 면적의 ~8%에 지나지 않는 작은 표면적에도 불구하고, 전세계 해양 이산화탄소 흡수의 10 - 20%를 차지하므로 탄소 순환 연구에서 중요하다(Cai et al., 2006; Chen and Borges, 2009; Laruelle et al., 2010). 또한 일방적으로 증가하는 인류기원 CO2 농도로 인한 산성화의 피해뿐만 아니라 담수의 유입, 육상 유기물과 영양분의 수송과 그에 따른 분해, 연안 용승과 같이 다른 원인에 의한 산성화에 영향을 받기도 한다(Gattuso and Hansson, 2011; Takahashi et al., 2014; Xiong et al., 2020; Middelburg et al., 2020; Cai et al., 2021). 따라서 외해역보다 산성화에 취약할 가능성이 있으므로 완충역량을 파악하는 것이 필요하다.
Table 1.
A list of six buffer factors used in this study (after Egleston et al., 2010)
| Response to Change in DIC | Response to Change in Alk |
연구해역인 한국 남부해역은 북서 태평양에 위치한 주변해로서 서쪽의 중국 대륙에서 장강이 유입되고, 남쪽에서 외양 기원 난류수가 북상하며, 연안 용승이 발생하는 등 수문학적 특징이 복잡하다(Park, 1986). 따라서 탄산계의 완충역량 또한 지역적 차이가 많이 날 것으로 예상됨에도 불구하고 이에 대한 연구가 이루어진 바 없다. 이에 더해 조사시기인 2020년 8월은 기후 변화가 야기한 기록적인 폭우가 발생하여, 기존의 장강 여름철(6, 7월) 월별 평균 강수량인 35mm의 약 4.3배인 150 mm를 기록한 바 있다(Zhou et al., 2021).
본 연구에서는 여러 산성화의 위협을 받고 있지만 연구가 많이 수행되지 않은 한국 남부해역 표층의 하계 완충역량을 계산하여 산성화에 저항하는 능력을 알아보았다. 또한 다양한 수문학적 요인으로 인해 범위가 넓은 수온, 염분과 해수 완충역량의 관계를 분석하여 연구해역의 환경적 요인이 완충역량에 미치는 영향을 고찰하였다.
2. 자료 및 방법
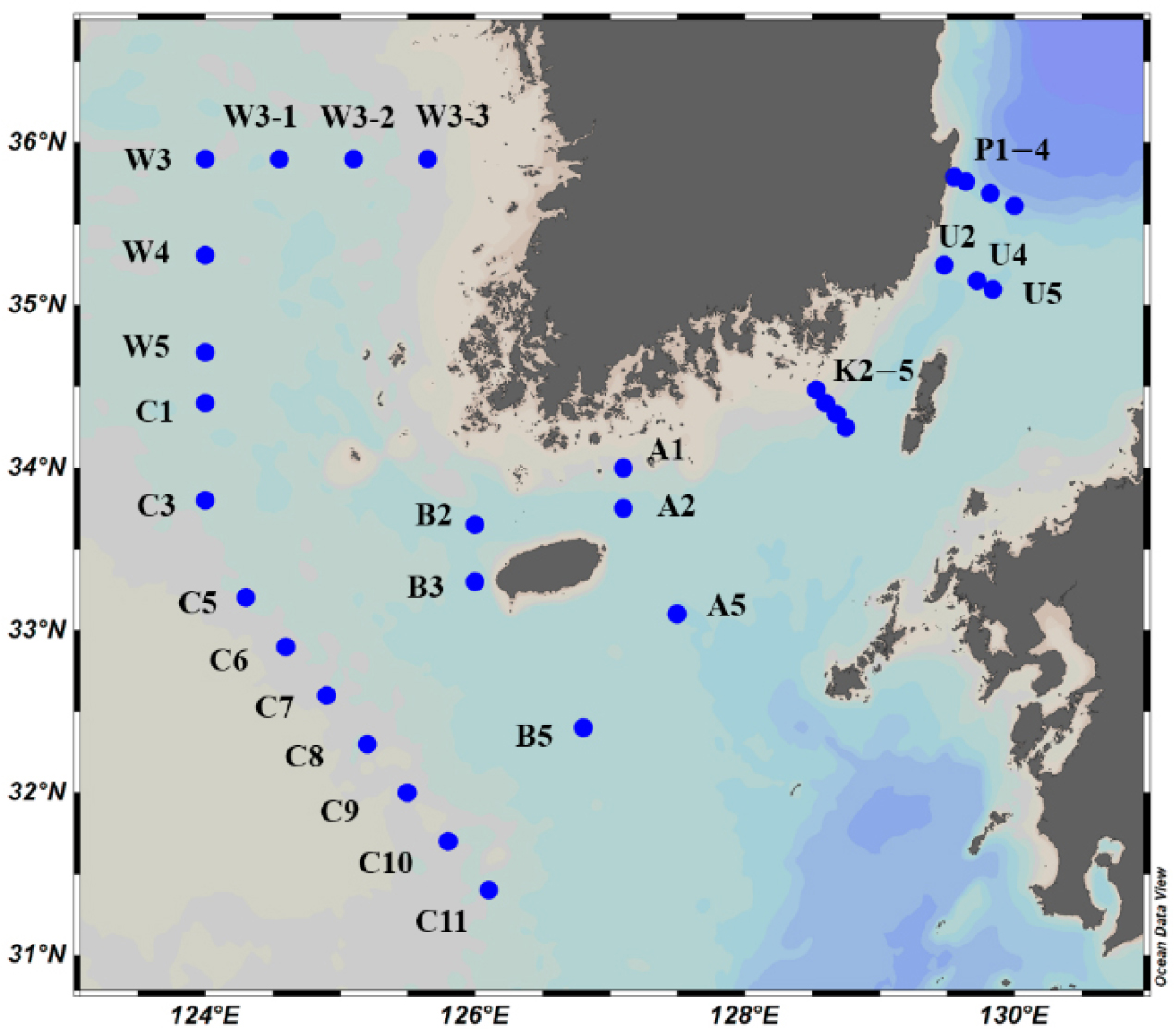
표층 완충역량 계산에는 황해, 동중국해 북부, 대한해협을 포함한 한국 남부해역의 2020년 8월 온누리호 조사 자료를 사용하였다(Fig. 1). 모든 정점에서 전 수심의 해수 시료가 채집되었으며, 그 중 표층에 해당하는 자료만 사용하였다. 표층, 즉 혼합층은 수심에 따른 수온이나 밀도의 변화가 거의 없는 준균질한(quasi-homogeneous) 영역이라는 정의에 근거하여(Roden, 1979; Pickard and Emery, 1990; Monterey and Levitus, 1997), 수온의 연직 분포가 일정한 수심 12 m 이내의 자료를 사용하였다. 그 결과 32개의 정점에서 표층으로 정의된 시료의 수는 총 60개였고, 정점별 평균값을 연구해역 표층의 완충역량으로 사용하였다.
CTD-rosette 시스템이 측정한 수온과 염분 그리고 CTD-Niskin 시스템에서 채수하여 분석한 DIC, TA를 사용하였다. DIC와 TA 분석을 위한 해수 시료는 선상의 CTD-Niskin으로부터 500 ml 용량 붕규산 병에 내려 받았으며, 생물활동에 의한 변질을 방지하기 위하여 200 µl의 포화 염화수은(HgCl2)을 주입한 후 밀봉하여 실험실로 운반하였다. 시료의 DIC, TA는 VINDTA 3C로 측정하였다. TA는 염산을 사용한 전위차 적정법(potentiometric titration)으로 측정하였으며, DIC는 인산으로 산성화시킨 후 방출된 이산화탄소 기체의 총량을 전기량계(coulometer)로 측정하였다. 측정된 DIC와 TA는 Scripps Institution of Oceanography의 Dickson lab에서 제공하는 인증표준물질(CRM)을 사용하여 보정하였다. 채수와 분석을 포함한 전 과정은 해양 이산화탄소 분석 지침서(Dickson et al., 2007)를 따랐으며, DIC, TA의 반복 측정 오차는 약 2 μmol kg-1이다.
Egleston et al.(2010)의 각 완충인자는 표층의 수온, 염분, DIC, TA를 CO2SYS.XLS (Lewis and Wallace, 1998) 프로그램에 입력하여 탄산계 화학종들의 농도를 구한 후 계산하였다. 탄산의 해리상수 K1, K2는 Dickson and Millero(1987)에 의해 수정된 Mehrbach et al.(1973)의 값을 사용하였다. 붕산의 해리상수인 Khb는 Dickson(1990)의 식을 참고하였다. 완충역량의 최종 단위는 mmol kg-1 이다. DIC 또는 TA와 탄산계 화학종(CO2, H+, ) 사이의 관계에 따라 6가지 완충인자들이 양수와 음수로 나뉘는데, 절대값이 클수록 완충역량이 크므로 이후로의 완충인자 값은 모두 절대값으로 제시하였다.
해수의 완충역량은 DIC/TA 비가 결정하며, 비가 낮을수록 완충역량이 더 크다(Chou et al., 2009; Egleston et al., 2010; Cai et al., 2020; Middelburg et al., 2020). 용존무기탄소(dissolved inorganic carbon; DIC)와 총 알칼리도(total alkalinity; TA)는 각각 다음과 같이 단순화할 수 있다(Zeebe and Wolf-Gladrow, 2001):
이때 해수 완충역량의 주 화학종인 는 아래의 식으로 표현된다:
이를 DIC/TA 비로 유도하면 다음과 같다:
DIC/TA 비가 낮다는 것은 []가 크다는 것이고, 가 많다는 것은 더 많은 CO2와 H+의 중화, 즉 강한 완충역량을 뜻한다. 따라서 큰 완충역량은 근본적으로 낮은 DIC/TA 비에 의한 것이다.
3. 결과 및 토의
3.1 표층 수온, 염분, 탄산계 매개변수, 탄산이온의 분포
완충인자의 계산에 사용한 수온, 염분과 같은 수문학적 요인들과 DIC, TA, DIC/TA 비와 같은 탄산계 매개변수들, 그리고 일차적 완충을 제공하는 []의 표층 분포를 Fig. 2에 나타냈다. 완충역량의 공간적 분포를 설명하기 위해 연구해역의 표층 수괴를 수온과 염분에 따라 다음의 5개로 나누었다: 동중국해 북부 표층에서 장강 유출수와 해수가 혼합되어 가장 저염한(S≤30) 장강희석수(Changjiang Diluted Water; CDW; Limeburner et al., 1983), 제주도 주변에서 고온인 대마난류수(Tsushima Warm Current; TWC), 중간 정도의 수온과 염분(T>24°C, S<32)을 갖는 황해표층수(Yellow Sea Surface Water; YSSW; Hur et al., 1999), 낙동강과 섬진강 등의 유입으로 염분이 낮고 저층수의 용승으로 수온이 낮은 남해표층혼합수(South Sea Surface Mixed Water; SSMW), 그리고 연안 용승으로 저온고염의 특징을 가진 동해표층혼합수(East Sea Surface Mixed Water; ESMW). SSMW와 ESMW는 하계의 계절적 용승에 의해 수온이 낮게 변형된 수괴이다.
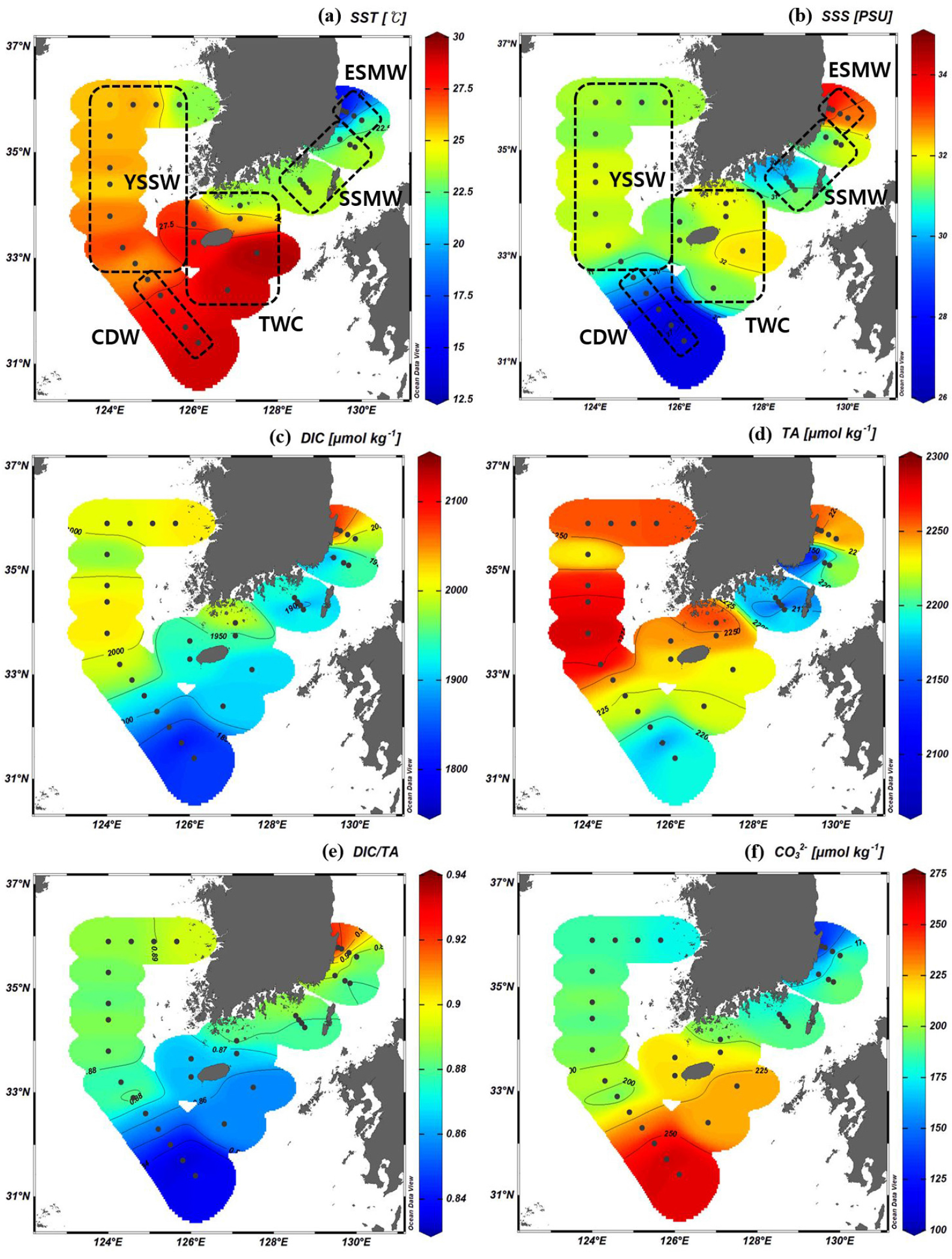
Fig. 2.
Spatial distributions of (a) sea surface temperature (SST), (b) sea surface salinity (SSS), (c) dissolved inorganic carbon (DIC), (d) total alkalinity (TA), (e) DIC/TA, (f) [] of southern Korean waters in August 2020. Black dots designate the sampling stations. YSSW: Yellow Sea Surface Water, CDW: Changjiang Diluted Water, TWC: Tsushima Warm Current, SSMW: South Sea Surface Mixed Water, ESMW: East Sea Surface Mixed Water.
표층의 여러 특성들은 수괴에 따라 뚜렷하게 대비되는 공간 분포를 보였다(Table 2). 수온은 14.0−29.4°C의 범위를 가지며, CDW와 TWC에서 높았고 ESMW에서 가장 낮았다. 염분의 범위는 26.8−34.2 psu로, 강물이 유입되는 CDW와 SSMW에서 낮았고 ESMW에서 가장 높았다. DIC의 범위는 1792−2120 μmol kg-1이며 강물로 희석되는 CDW, SSMW와, 고온인 TWC에서 작은 값을 보였다. 또한 연안 용승으로 DIC가 풍부한 심층수가 용승하는 ESMW가 가장 큰 값을 가졌다. TA는 2061−2283 μmol kg-1의 범위를 보였다. 외양 표층의 TA는 염분과 비례하며(Broecker and Peng, 1982; Millero et al., 1998), 강물 유입 영향으로 염분이 낮은 CDW와 SSMW에서도 TA가 작았다. 하지만 염분의 평균이 31.5 ± 0.2 psu로 상대적으로 높지 않은 YSSW에서 TA가 가장 컸다. 이는 집중적인 탄산칼슘 광물의 풍화와 침식으로 약 2874−3665 μmol kg-1의 TA를 갖는 황하가 황해로 유입되기 때문이다(Chou et al., 2009). 이러한 DIC와 TA의 분포에 따라 DIC/TA 비의 범위는 0.83−0.93으로 나타났으며, CDW와 TWC에서 낮았고, ESMW에서 높았다. []는 118−265 μmol kg-1의 범위를 가졌으며 식 (5)에 의해 DIC/TA 비와 역상관 분포를 보였다.
Table 2.
Mean and one standard deviation of temperature, salinity, DIC (dissolved inorganic carbon), TA (total alkalinity), DIC/TA, [] for each water mass in the southern Korean surface waters
| CDW1 | TWC2 | YSSW3 | SSMW4 | ESMW5 | |
| SST (°C) | 28.0 ± 1.0 | 27.2 ± 2.1 | 25.6 ± 1.0 | 23.2 ± 0.8 | 18.5 ± 3.8 |
| SSS (psu) | 28.3 ± 1.3 | 31.6 ± 0.3 | 31.5 ± 0.2 | 31.0 ± 1.0 | 33.2 ± 0.6 |
| DIC (μmol kg-1) | 1862 ± 42 | 1938 ± 28 | 2002 ± 15 | 1919 ± 58 | 2037 ± 57 |
| TA (μmol kg-1) | 2202 ± 20 | 2240 ± 12 | 2261 ± 15 | 2174 ± 60 | 2248 ± 17 |
| DIC/TA | 0.845 ± 0.012 | 0.865 ± 0.008 | 0.885 ± 0.004 | 0.883 ± 0.007 | 0.906 ± 0.021 |
| [] (μmol kg-1) | 246 ± 17 | 217 ± 11 | 190 ± 7 | 184 ± 11 | 155 ± 31 |
3.2 완충인자들의 표층 분포
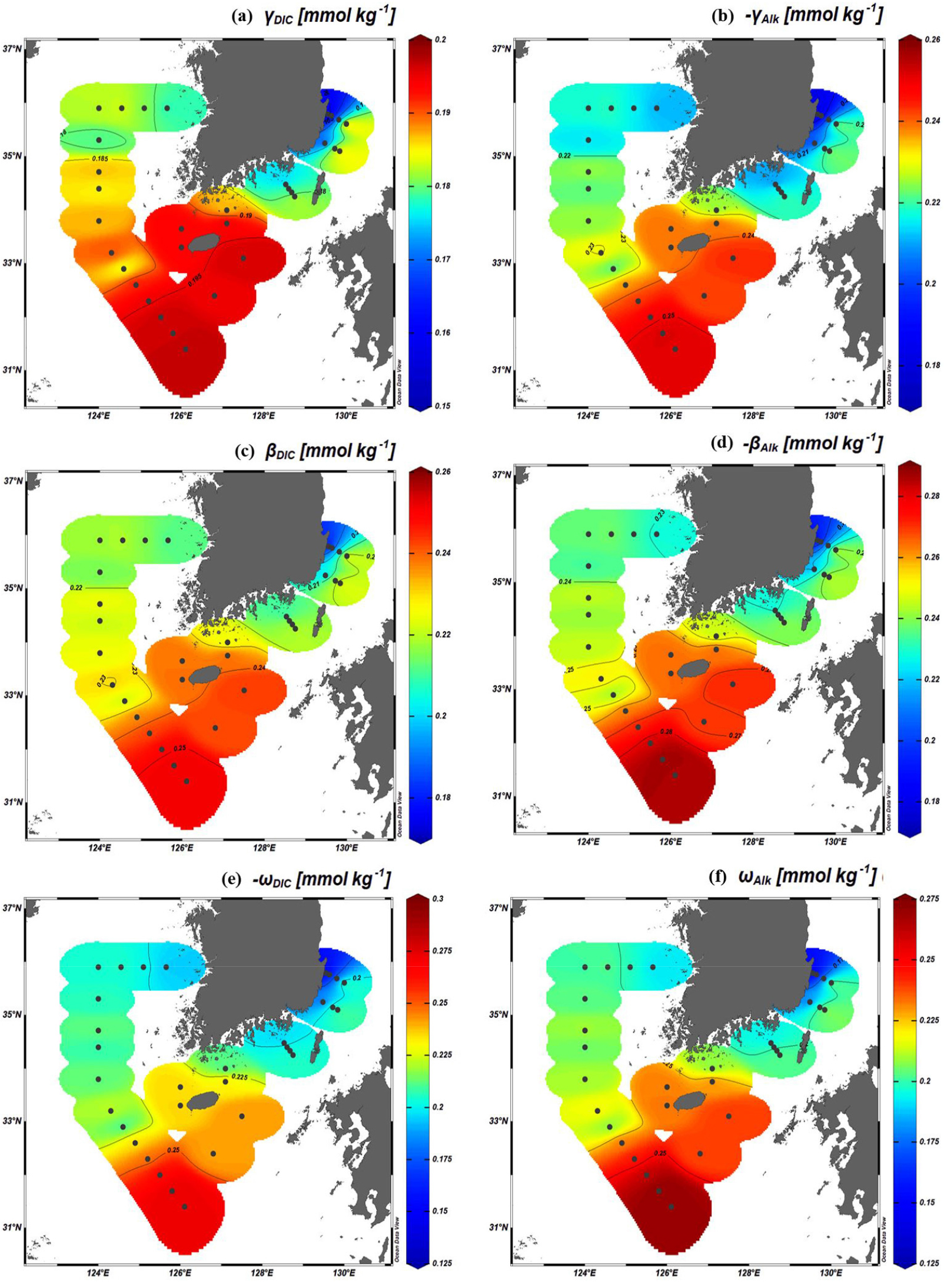
Egleston et al.(2010)의 6가지 완충인자들은 CDW와 TWC에서 크고 SSMW, ESMW에서 작은 공간적으로 닮은 분포를 보였다. 또한 수괴에 따른 분명한 차이가 나타났는데, 모두 ESMW, SSMW, YSSW, TWC, CDW 순으로 증가하여 CDW에서 가장 컸다(Fig. 3, Table 3). 6가지 완충인자들의 공간적 분포는 비슷할 수밖에 없다. DIC 또는 TA의 변화에 대한 [] 변화의 저항을 나타내는 가 크면 []의 소모율이 작다는 것을 의미하고, 의 소모율이 작으면 더 많은 [CO2]()와 [H+]()의 변화를 완충할 수 있기 때문이다. 따라서 이후로는 Revelle 인자와 가장 가까운 를 완충역량의 대표로 논의하였다.
Table 3.
Mean and one standard deviation of six buffer factors for each water mass of the southern Korean sea in August 2020
| Buffer factor | Water mass1 | Mean ± 1 standard deviation (mmol kg-1) |
|
ESMW SSMW |
0.170 ± 0.014 0.179 ± 0.007 | |
| YSSW | 0.184 ± 0.003 | |
| TWC | 0.193 ± 0.003 | |
| CDW | 0.195 ± 0.002 | |
|
ESMW SSMW |
0.199 ± 0.022 0.215 ± 0.009 | |
| YSSW | 0.220 ± 0.005 | |
| TWC | 0.238 ± 0.006 | |
| CDW | 0.247 ± 0.006 | |
|
ESMW SSMW |
0.199 ± 0.022 0.215 ± 0.009 | |
| YSSW | 0.220 ± 0.005 | |
| TWC | 0.238 ± 0.006 | |
| CDW | 0.247 ± 0.006 | |
|
ESMW SSMW |
0.213 ± 0.028 0.234 ± 0.011 | |
| YSSW | 0.240 ± 0.007 | |
| TWC | 0.263 ± 0.009 | |
| CDW | 0.278 ± 0.009 | |
|
ESMW SSMW |
0.176 ± 0.028 0.200 ± 0.010 | |
| YSSW | 0.208 ± 0.007 | |
| TWC | 0.233 ± 0.011 | |
| CDW | 0.259 ± 0.016 | |
|
ESMW SSMW |
0.173 ± 0.028 0.198 ± 0.010 | |
| YSSW | 0.205 ± 0.007 | |
| TWC | 0.230 ± 0.011 | |
| CDW | 0.256 ± 0.016 |
3.3 수온, 염분과 완충역량의 관계
해수의 완충역량을 결정하는 DIC와 TA는 광합성 또는 호흡과 같은 생지화학적 과정, 연안 용승, 강물의 유입, 수직적 또는 수평적인 혼합, 그리고 수온 변화 등에 의해 변하며, DIC의 경우에는 대기와의 기체 교환도 중요하다(Takahashi et al., 2014; Xiong et al., 2020; Middelburg et al., 2020; Cai et al., 2020, 2021). 연구해역은 다양한 수괴의 영향으로 특히 환경적 요인인 수온과 염분의 변동성이 크므로 이들과 완충역량의 관계를 알아보기 위해 선형 회귀 방법을 사용하였다.
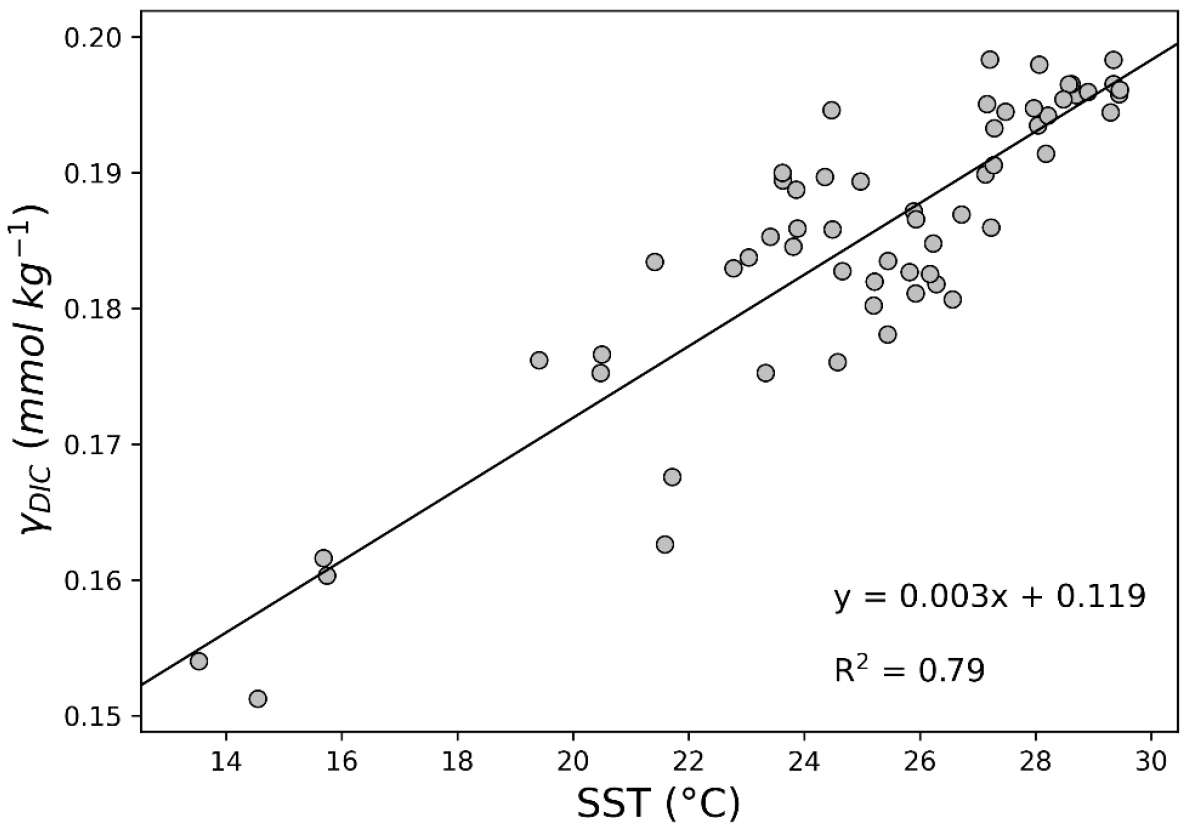
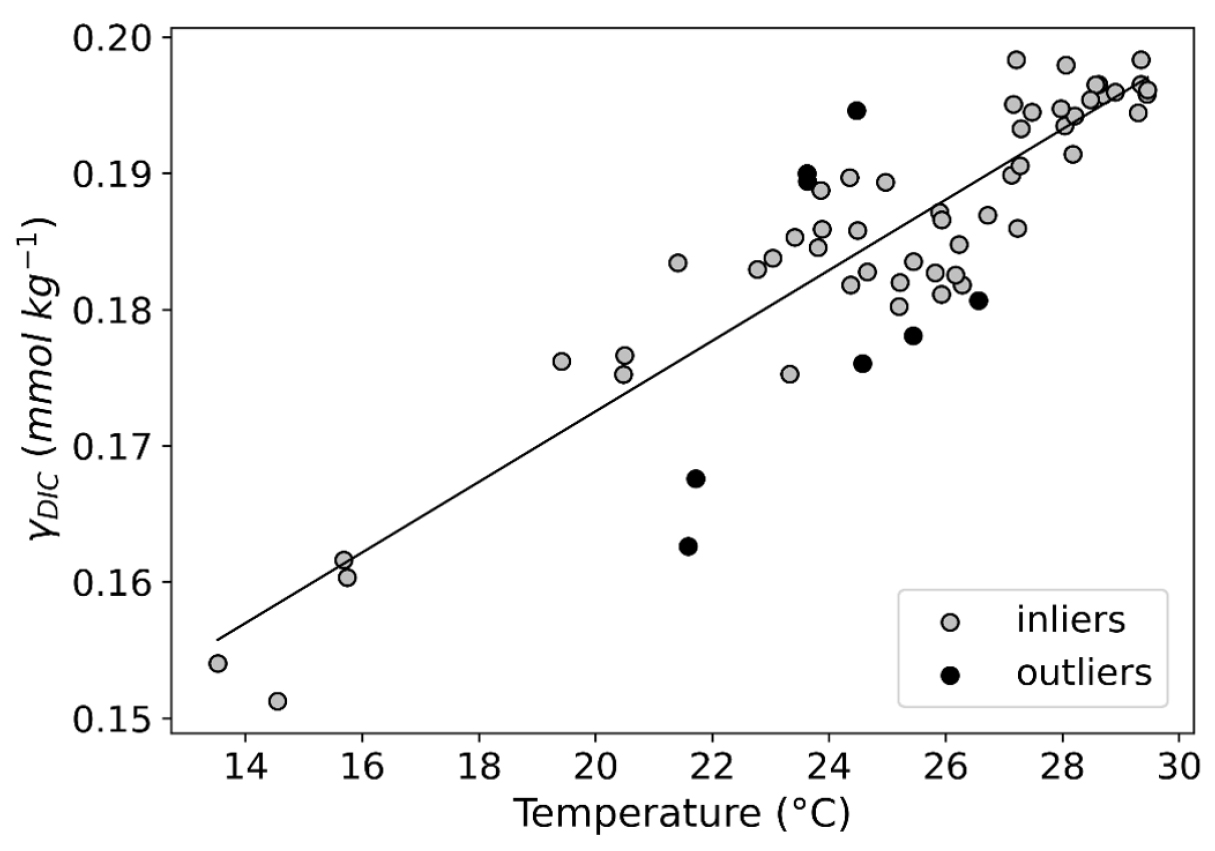
수온-완충역량은 R2=0.79인 유의한 양의 상관관계를 보였다(Fig. 4). 수온은 주로 두 가지 과정을 통해 해수의 탄산계를 조절한다: 대기-해양의 CO2 기체 평형을 통해 해수의 DIC/TA 비를 변화시키는 과정과, 탄산계의 화학적 종 분화에 영향을 미치는 과정이다(Jiang et al., 2019; Cai et al., 2020, 2021). 먼저 수온에 민감한 대기-해양의 CO2 기체 평형 과정이다. 대기에서 기체 상태로 존재하는 CO2는 해수에 용해되어 용존 CO2가 된다.
식 (6)에서 K0는 CO2의 용해도(solubility) 상수이다. 수온, 염분, 압력이 용해도 상수에 영향을 주는데, 본 연구에서는 표층만 다루므로 압력의 변화는 없다고 가정한다. 용해도 상수에 대한 수온의 영향만을 보기 위해 특정 염분에 대해 정규화(normalize)를 했을 때, 수온이 상승하면 K0가 감소하고, 이산화탄소 분압인 pCO2(=[CO2(aq)]/K0)가 증가하여 해수 속 CO2를 대기로 방출시킨다. CO2가 방출되면 DIC는 감소한다. 따라서 수온이 오르면 대기-해양 기체 교환은 DIC/TA 비를 낮춰 완충역량을 강화한다.
두 번째 과정은 해수에 녹아 있는 탄산계 화학종의 조성비를 변화시켜 완충역량에 영향을 미친다. 탄산의 첫 번째, 두 번째 해리상수인 K1(= [H+][H]/[H2CO3],), K2(= [H+][]/[H])에 의해, K1/K2는 대기중 CO2가 해수에 용해되어 겪는 순 산-염기 반응 식 (7)의 평형상수가 된다.
K0와 마찬가지로 일정한 염분과 압력에서 수온이 상승하면 K1/K2 또한 감소하여 식 (7)에서 왼쪽으로의 반응을 선호하게 되고, H가 CO2와 로 전환된다. 높은 수온이 를 늘려 완충역량을 증가시키는 것이다.
수온의 상승이 탄산계에 일으키는 두 과정이 모두 완충역량을 강화하지만, K0가 K1/K2보다 온도 변화에 더 민감하다(Cai et al., 2021). 따라서 대기-해양 기체 교환 과정의 기여도가 더 클 것이라고 예상할 수 있다. 그러나 대부분의 기체가 대기-해양 평형을 이루는 데 몇 주면 충분한데 반해 CO2는 최소 한 달에서 수 개월이 필요하다(Broecker and Peng, 1974; Zeebe and Wolf-Gladrow, 2001; Gattuso and Hansson, 2011; Cai et al., 2021). 이러한 시간의 지연없이 수온의 높고 낮음이 즉각적으로 DIC/TA 비에 반영이 되는 이유에 대해서는 추후 연구가 필요한데, 일차적으로는 혼합층의 두께가 얇은 것이 원인을 제공한다.
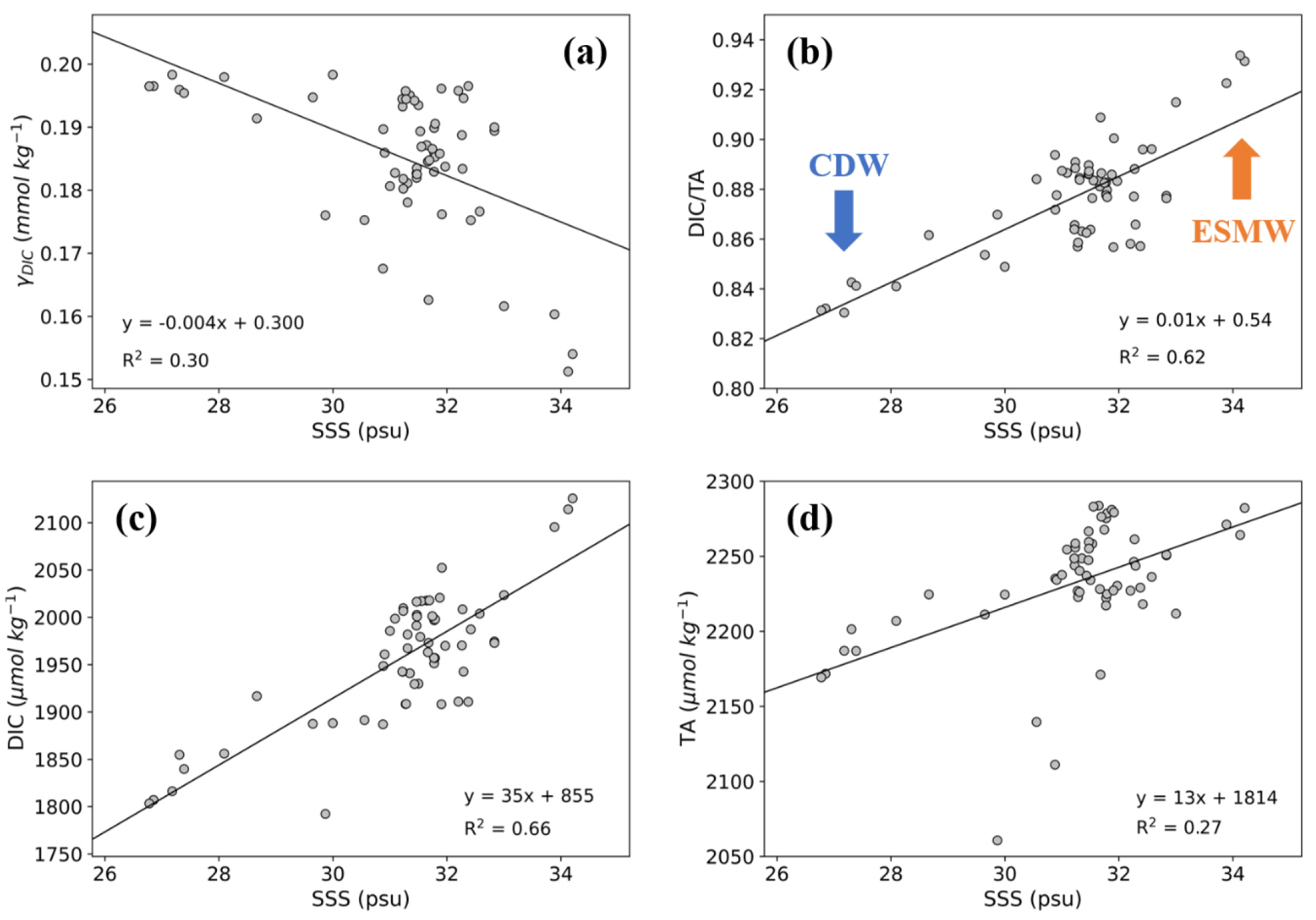
다음은 완충역량과 염분의 관계이다. 수온의 영향을 제거하기 위해 용해도 상수와 평형 상수를 특정 수온에 대해 정규화 했을 때 염분이 증가하면 K0와 K1/K2가 모두 감소하므로(Cai et al., 2021), 수온과 마찬가지로 완충역량과 양의 관계를 가질 것이라고 예측할 수 있다. 그러나 연구해역에서 염분-완충역량은 R2=0.30인 약한 음의 관계를 보였다(Fig. 5(a)). 원인을 규명하기 위해 완충역량을 결정하는 DIC/TA 비와 DIC, TA 각각을 염분과 선형 회귀하였다. 염분-DIC/TA는 R2=0.62인 유의한 양의 관계를 보여주며, 염분-DIC는 R2=0.66인 양의 관계, 염분-TA는 R2=0.27인 약한 양의 관계를 가지는 것에서 염분-DIC의 관계가 염분-완충역량을 주도하는 것을 알 수 있다(Fig. 5(b), (c), (d)). 일반적으로 염분이 증가하면 K0가 감소하므로 염분-DIC는 음의 관계를 가져야 한다. 그러나 염분-DIC가 양의 관계를 보이는 이유는 연구해역의 표층 염분의 변화가 증발이나 강수보다는 CDW, ESMW 등의 수괴의 유입에 영향을 받기 때문이다. CDW는 주변 해수보다 염분과 DIC가 낮고, ESMW는 염분과 DIC가 높으므로(Fig. 2, Table 2) 염분-DIC/TA 비 사이에 양의 상관관계가 생겼다. 그러나 실제로 염분이 DIC/TA 비를 조절하는 것이 아니라 교란하므로 염분과 완충역량 사이에 약한 음의 상관관계가 나타난 것으로 해석된다.
수괴마다 고유한 값을 가지는 수온과 염분이 모두 완충역량과 유의한 상관관계를 갖지 않고, 수온만 상관도가 높은 것에서 수괴의 특성이 완충역량을 조절하는 것이 아니라 수온 자체가 중요하다는 것을 알 수 있다.
염분은 완충역량과 상관관계가 미약하므로 수온만으로 완충역량을 예상하는 회귀 모델을 만든 후, 이상점(outlier)을 찾아내고 분석하여 수온만으로 예측이 어려운 데이터들을 살펴보았다. RANSAC (RAndom SAmple Consensus) 알고리즘을 사용하여 데이터와 회귀 직선 사이의 수직 거리가 y값()의 중앙값 절대 편차(median absolute deviation)를 넘어서는 데이터를 이상점으로 분류하였다. 연구해역의 표층에서 총 8개의 자료가 이상점으로 분류가 되었다(Fig. 6). 각 이상점들의 정보(정점, 수심, 수온, 염분)와 이상점이 속하는 수괴, 그리고 그 수괴의 평균 수온, 염분을 Table 4에 제시했다. 다수의 이상점은 육지 근처에 존재한다. 난류수의 영향으로 모델의 예측보다 큰 완충역량을 갖는 3개소(A2, P4)를 제외하고, 나머지 5개는 모델의 예측보다 확연히 작은 완충역량을 가진다. 그 중 대부분은 육지로부터 직접적으로 강물이 유입되는 SSMW 수괴의 K와 U 관측선의 것으로(Fig. 1), 해수보다 DIC/TA 비가 훨씬 높아 []가 낮은 담수의 유입이 를 희석시켜 농도를 낮추기 때문으로 추측된다(Gattuso and Hansson, 2011; Cai et al., 2020, 2021). 또한 부근의 ESMW 수괴에서 발생하는 연안 용승의 영향도 있을 것이다. 연안역과 외해역 사이에 열염전선이 형성되어(Fig. 2(a), (b)) 외해역과 제한적으로 해수가 교환되는 연안의 특성도 완충역량을 낮추는 데 일조했을 것으로 판단된다. 결과적으로 이상점들은 연구해역의 연안역이 외해역보다 산성화에 취약할 수 있으므로 혼합 특성을 포함한 별도의 집중적인 연구가 필요함을 시사한다.
Table 4.
The water mass-specific outliers with station number, depth, temperature, salinity (see Fig. 1 for station location). For comparison the mean temperature and salinity of each water mass are also listed
| Water mass1 | Mean Temperature (°C) / Salinity (psu) | Outliers | ||
| Stations |
Sampling Depths (m) | Temperature (°C) / Salinity (psu) | ||
| TWC | 27.2 / 31.6 | A2 | 10 | 24.5 / 32.3 |
| YSSW | 25.6 / 31.5 | W3-3 | 2 | 26.6 / 31.0 |
| W4 | 11 | 25.4 / 31.3 | ||
| SSMW | 23.2 / 31.0 | K2 | 10 | 21.6 / 31.7 |
| K4 | 2 | 24.6 / 29.9 | ||
| U2 | 2 | 21.7 / 30.9 | ||
| ESMW | 18.5 / 33.2 | P4 | 2 | 23.6 / 32.8 |
| 10 | 23.6 / 32.8 | |||
3.4 수괴별 완충역량
2020년 8월 표층 수괴들의 완충역량은 ESMW, SSMW, YSSW, TWC 그리고 CDW의 순으로 컸다(Fig. 3, Table 3). CDW의 큰 완충역량(=0.195 ± 0.002 mmol kg-1)은 생물학적 생산이 주원인으로 추정된다(Tsunogai et al., 1997, 1999; Wang et al., 2000, Shim et al., 2007; Xiong et al., 2019). 영양염은 풍부하지만 탁도가 높아 생산성이 낮은 강물은 탁도가 낮아 광합성을 하기에 충분한 양의 빛이 투과하는 해양과 만나며 생산력이 높아지게 된다. 다음 식과 같이 광합성이 일어날 때 이산화탄소와 영양염이 소모된다(Redfield et al., 1963):
이산화탄소의 소모는 DIC를 감소시키고, 영양염의 소비는 TA를 증가시키므로(Wolf-Gladrow et al., 2007) DIC/TA 비를 낮춘다. 실제로 장강의 내륙부에서 > 1.0인 DIC/TA 비는 하구 근처에서 최대 0.8까지 낮아지고, 일반적으로 0.8−0.9의 값을 가진 해수와 혼합되며 CDW의 DIC/TA 비를 낮춘다(Xiong et al., 2019). DIC/TA 비의 감소는 완충역량을 강화한다. 또한 수온과 완충역량이 양의 상관관계를 가지므로 평균 수온이 28.0 ± 1.0°C로 수괴 중 가장 높은 것도(Table 2) 완충역량의 제고에 영향을 미쳤을 것이다. 하계의 강한 성층화로 인해 DIC가 풍부한 심층수와의 연직 혼합이 약화된 것도 원인 중 하나이다(Chou et al., 2009).
이러한 이유들로 큰 CDW의 완충역량은 장강유출수가 연구해역의 완충역량을 강화한다는 것을 시사한다. 이를 확인하기 위해 황해 표층(1−6 m)의 탄산계를 다룬 Wang and Zhai(2021)에서 CDW의 영향을 받는 남부역(Southern South Yellow Sea)의 월별 수온, 염분, DIC, TA 자료를 사용하여 완충역량을 계산해서 본 연구의 값과 비교하였다(Fig. 7). 이 연구의 결과인 2020년 8월의 값은 빨간 세모로 표시하였다. 장강유출수의 유입으로 염분이 낮아지고 DIC, TA가 희석되며, 수온은 높아지는 여름으로 갈수록 완충역량이 증가하다가, 장강의 영향이 줄어들고 수온이 낮아지는 가을과 겨울을 거치며 점점 완충역량이 감소하여 4월에 가장 낮다. 또한 기록적인 폭우가 내렸던 2020년 8월의 염분이 가장 낮으며 완충역량이 가장 크다. 따라서 장강유출수는 연구해역의 완충역량을 확실히 보강하는 방향으로 기여하는 것으로 보인다.
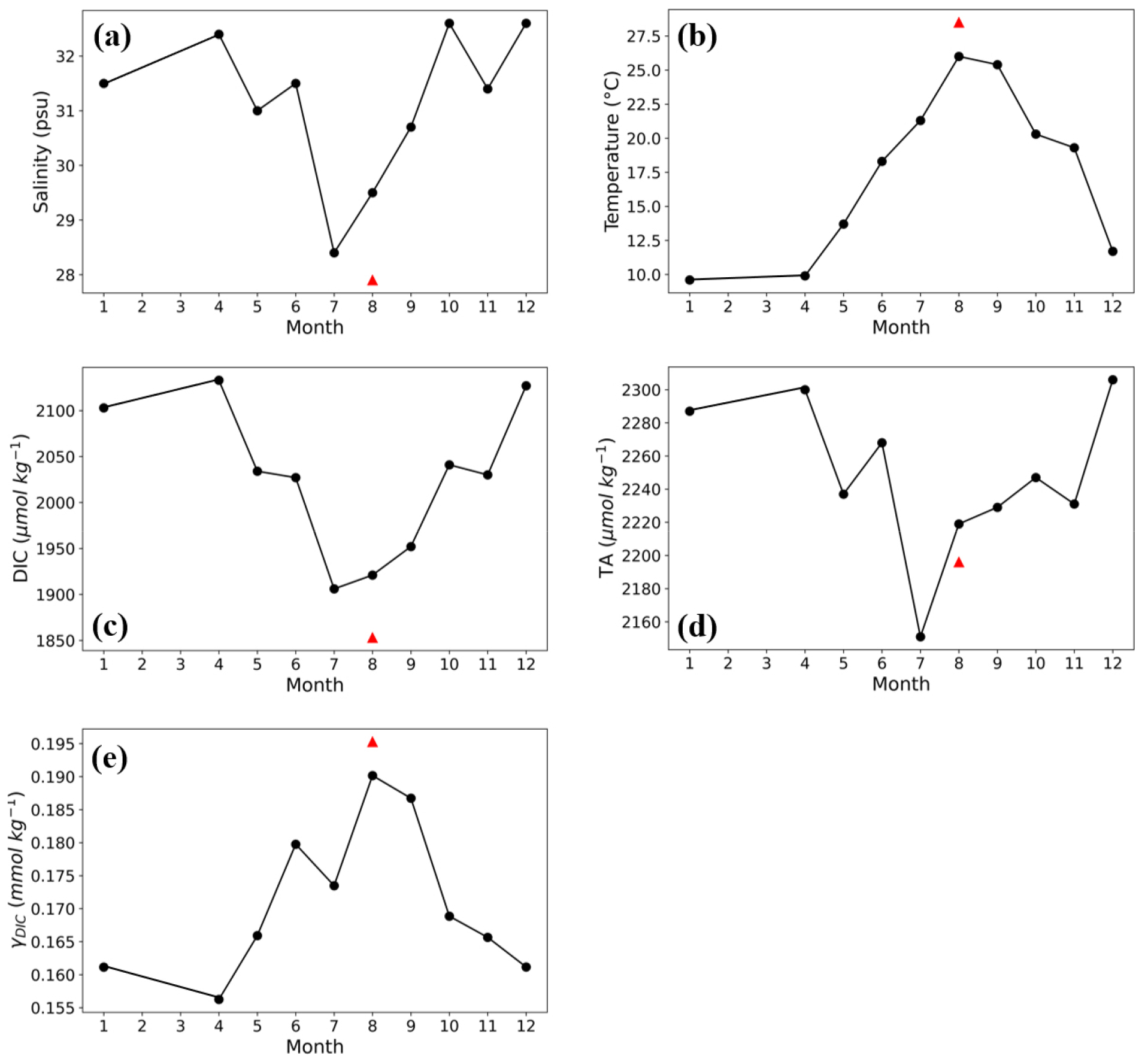
Fig. 7.
Monthly variations of (a) salinity, (b) temperature, (c) dissolved inorganic carbon (DIC), (d) total alkalinity (TA), (e) of Southern Yellow Sea from Wang and Zhai (2021). Salinity, temperature, DIC, TA, and of Changjiang Diluted Water (CDW) in this study are represented by red triangles.
TWC의 평균 완충역량()은 0.193 ± 0.003 mmol kg-1으로 CDW 다음으로 크지만, 빈영양이어서 생산력이 낮다. 그럼에도 불구하고 완충역량이 두 번째로 큰 이유는 쿠로시오 기원으로 높은 수온(27.2 ± 2.1°C)과 풍부한 TA (2240 ± 12 μmol kg-1)가 DIC/TA 비를 낮추기 때문으로 해석된다(Fig. 2(a), (d), Table 2). 수온은 앞에서 설명한 두 가지 과정을 통해 DIC/TA 비를 낮추며, 외양 기원수의 표층 TA는 염분과 정비례하므로 TWC의 높은 TA 또한 DIC/TA 비를 낮춘다.
연구해역에서 중간 정도의 완충역량(=0.184 ± 0.003 mmol kg-1)을 갖는 YSSW 또한 동중국해 대륙붕에 비해 훨씬 낮은 생산력을 가진다(Qu et al., 2015). 따라서 완충역량을 높이는 다른 원인이 있으며, 높은 TA가 그 원인으로 지목된다(Fig. 2(d), Table 2). 황하가 유입되는 YSSW의 평균 TA는 2261 ± 15 μmol kg-1로 쿠로시오 기원의 TWC보다 높다. 그러나 수온의 평균이 25.6 ± 1.0°C로 높지 않아(Table 2) TWC보다 낮은 완충역량을 가진다.
SSMW와 ESMW의 평균 는 각각 0.179 ± 0.007 mmol kg-1, 0.170 ± 0.014 mmol kg-1로 낮다(Table 3). 이는 두 수괴가 모두 앞서 말했던 강물에 의한 []의 희석과, DIC가 풍부한 저층수의 용승 영향을 받기 때문이다. 수온약층 아래에 고립된 저층수는 수온이 매우 낮으며, 주로 호흡이 발생한다. 호흡은 식 (8)의 역반응으로서, DIC/TA 비를 높인다. DIC/TA 비가 증가하면 완충역량은 위축된다. SSMW와 ESMW의 평균 수온 또한 23.2 ± 0.8°C, 18.5 ± 3.8°C로 낮은 편이므로 완충역량을 낮춘다(Table 2).
4. 요 약
주변해인 한국 남부해역이 산성화에 저항하는 능력이 지금까지 알려지지 않았으므로 표층 수괴별 탄산계의 완충역량을 계산하고 그 값을 비교하였다. CDW의 매우 높은 완충역량은 장강유출수가 연구해역의 완충역량 강화에 기여함을 의미한다. 또한 생물학적 생산력과 높은 수온이 주원인, 하계의 강한 성층화가 보조 원인으로 판단된다. 외양 기원이며 고온인 TWC는 두 번째로 완충역량이 높았으며, YSSW는 중간값을 가지고, 저층수의 용승이 발생하는 SSMW, ESMW의 완충역량은 낮았다.
발표된 황해의 DIC와 TA 월별 자료를 토대로 분석한 완충역량 결과로부터 Keeling curve와 거울상인 변화를 발견하였다. 완충역량은 봄에 가장 낮고 여름 후반기에 가장 높을 것으로 예상된다.
하계에 수온과 완충역량은 수괴와 상관없이 강한 양의 상관관계를 보인데 반해 염분은 상관성이 낮았다. 이는 연구해역의 염분이 국지적인 수괴와의 혼합에 의해 변하여 염분과 해수 탄산계의 보편적인 관계가 교란되었기 때문이다. 결론적으로 한국 남부 해역의 완충역량은 DIC/TA 비가 지배 요인이며 수온은 열역학적 과정을 통해 DIC 농도를 결정한다. 또한 DIC 배경 농도를 교란시키는 과정인 용승과 장강을 위시한 대규모 담수 유입이 지리적 분포를 결정한다.
표층의 완충역량 이상점 분석 결과는 연안역이 외해역보다 산성화에 취약할 수 있으며, 열염전선의 형성으로 인해 외해역과의 혼합 또한 제한적이므로 별도의 집중적인 연구가 필요하다는 것을 지적한다.