1. 서 론
2. 메탄의 생지화학적 거동
2.1 메탄 저장소
2.2 미생물에 의한 메탄 형성의 생지화학적 과정
2.3 해수 내 메탄 생성(메탄 역설)
2.4 퇴적층에서 메탄 생성
2.5 해양 퇴적층 내 메탄 생성
2.6 담수와 육상지역에서 메탄 생성
3. 메탄 제거
3.1 유산소 메탄 제거(Aerobic methane oxidation)
3.2 무산소 메탄 산화(Anaerobic methane oxidation)
4. 해양 저산소층 발달과 메탄 생성
4.1 한국 내 해수 저산소층 분포
4.2 진해 당동만의 성층과 빈산소에 따른 퇴적물내 혐기층 발달과 메탄
5. 결 론
1. 서 론
메탄은 화학 구조상 가장 단순하고 안정적인 n-Alkanes 탄화수소물(hydrocarbon)이고, 대부분 미생물활동으로 생성되기 때문에, 지구상에서 가장 풍부한 유기 분자라고 알려져 있다(Thauer and Shima, 2008; Whiticar, 2020). 메탄은 지구 기후에 아주 중요한 역할을 하는데, 기후변화에 관한 정부 간 패널(International Panel of Climate Change, IPCC) 보고서에 따르면, 최근 20년간 메탄의 온실효과는 같은 양의 이산화탄소에 비해 약 80배 이상 높다고 보고 하였다(Canadell et al., 2021). 또한, 메탄은 대기 중 햇빛 및 다른 물질과 반응하여, 오존 거동에 간접적으로 영향을 미치는 등 대기 화학에 아주 중요한 역할을 한다(Reeburgh, 2007; Valentine, 2011). 하지만, 메탄 연구는 같은 온실기체인 이산화탄소에 비해 많이 진행되어 있지 않다. 즉, 대기-물(해양 및 호수, 강) 기체교환이 얼마인지, 시공간에 따라 어떻게 변하는지, 어떤 생물이 생성 및 제거하는지 등은 잘 알려지지 않았다. 예를 들어, IPCC 보고서에서 자연발생 및 육상과 해상에서 지질적 요인으로 유출되는 메탄의 양은, Top-Down 방식에서는 0-71 Tg-CH4/yr(평균: 23 Tg-CH4/yr)으로 아주 광범위하게 추정하였다. 같은 항목의 Bottom-up 방식으로는 18-65 Tg-CH4/yr(평균: 45 Tg-CH4/yr)로 추정하여, 두 방식 간 유출량의 차이 또한 아주 크다(Canadell et al., 2021). 추정치 값의 아주 넓은 범위는 아직 많은 연구가 이루어져 있지 않기 때문이다(Weber et al., 2019). 특히, 한국의 경우, 해양에서 메탄 연구는 찾아보기 힘들다(e.g., Kim and An, 2022).
2. 메탄의 생지화학적 거동
메탄의 생지화학적 거동에 대해서는 Whiticar(2020), Reeburgh(2007), Valentine(2002, 2011), Hinrichs and Boetius(2003), Ruppel and Kessler(2017)등에 자세히 나타나 있고, 이 논문은 이들을 간추린 보고서이다. 자세한 내용은 위 논문들을 참조하길 바란다.
2.1 메탄 저장소
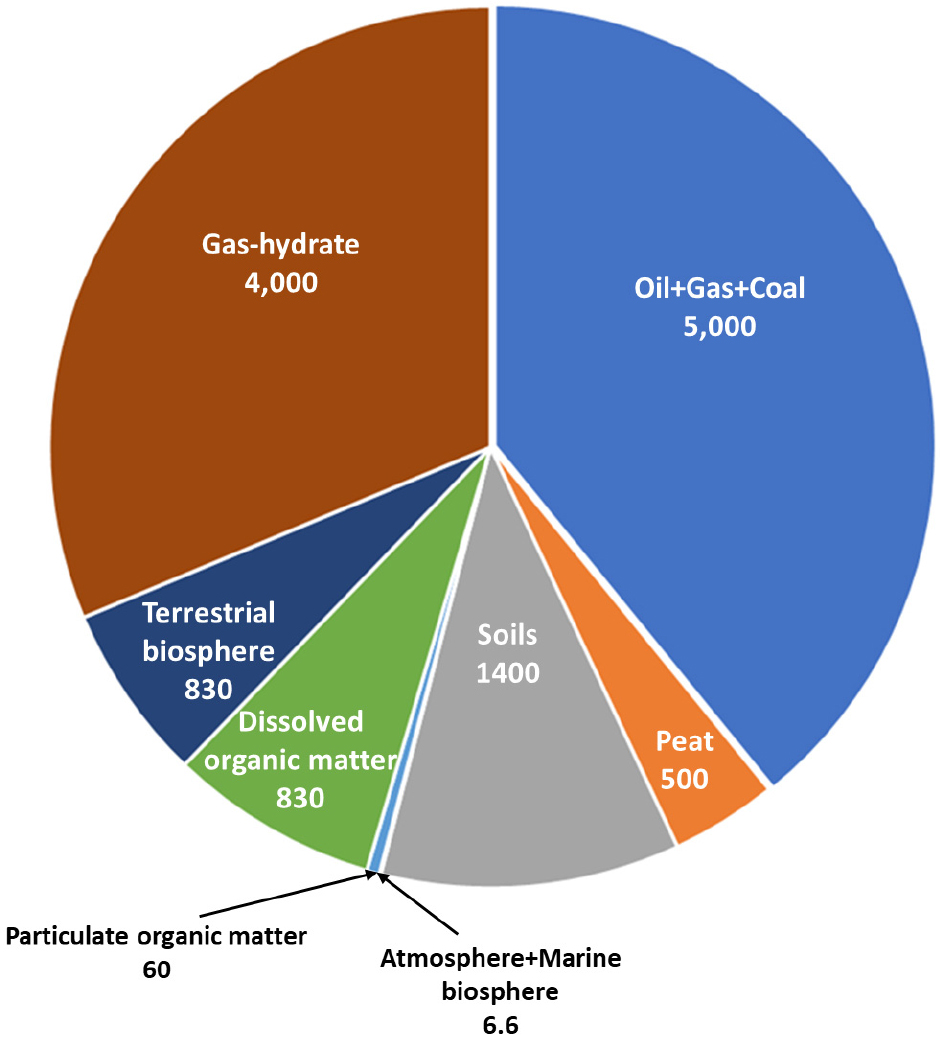
대부분의 메탄은 하이드레이트(hydrates) 형태로 존재하며(Whiticar, 2020; Majumdar et al., 2022), 깊은 해양(500 m 이하)에 주로 존재한다(Ruppel and Kessler, 2017). 하이드레이트는 물 분자가 결정화될 때(crystallization), 물 분자 사이 공간에 기체 분자가(guest molecules) 포획된 형태이며, 온도와 압력에 의해 그 안정성이 달라진다. 메탄 하이드레이트 경우, 극지방의 낮은 온도와 대양의 약 깊이 500 m 이하에서 비교적 안정적이다. 따라서, 해양 중층수의 온도 변화는 하이드레이트의 붕괴를 유발하여 메탄의 수층 및 대기 유입이 예상된다(Ruppel, 2011). 메탄 하이드레이트의 양은 약 5~36 x 105 Tg CH4로 추정된다(Milkov, 2005; Boswell and Collett, 2011; Wallmann et al., 2012). 이 양은, 모든 토양, 퇴적층, 용존 유기물 내 탄소량보다 크고, 원유, 천연가스, 석탄 내 탄소 양과 거의 같은 양이다(Fig. 1)(Whiticar, 2020). 또한, 현재 대기 메탄 총량(0.0485 x 105 Tg CH4 or, 1864 ppb) 보다 약 740 배 정도 많은 양이다. 이렇게 많은 양이 하이드레이트로 존재하기 때문에, 약 0.1%의 하이드레이트(예, 극지방 하이드레이트는 전체 양의 약 2~3%)가 붕괴되 대기로 유출된다면, 현재 대기 농도가 거의 2배 가까이 될 것으로 예상된다(Ruppel, 2011). 해수 내 용존 메탄은 약 43 Tg-CH4 로 추정되는데(Reeburgh, 2007), 이는 하이드레이트 메탄 보다 약 84,000 배 적은 양이다. 이렇게 많은 양이 해저에 존재하기 때문에, 일부 과학자들은, 약 55 mya 전 Paleocene-Eocene Thermal Maximum 시기 하이드레이트가 용해되어 메탄이 대기로 유출돼, 간빙기가 도래한 것으로 추정하고 있으나 정확한 원인과 과정은 밝혀지지 않았다(Dickens et al., 1995; Nisbet and Piper, 1998). 또한, Neoproterozoic hydrates가 불안정해져서, 지구 탄소 순환에 영향을 미쳤으리라 추정되기도 한다(Kennedy et al., 2001; Halverson et al., 2002).
2.2 미생물에 의한 메탄 형성의 생지화학적 과정
유기물의 분해 및 메탄 생성 과정을 Fig. 2에 표현하였다. 유기물은 박테리아에 의해 해리(hydrolysis)되어 올리고머(Oligomer) 및 단랑체(monomers)를 생성하고, 발효(fermentation) 과정을 통해 이산화탄소, 아세트산 등을 생성한다. 이후 메탄 생성 미생물(methanogenesis)에 의해 메탄이 생성된다. 이 무산소 유기물 분해 과정에서는 필수적으로 종속영양(heterotrophic) 미생물이 큰 유기물을 작은 유기물 혹은 메탄 생성 미생물이 사용할 수 있는 분자(예를 들어, acetate, CO2, 및 Methyl 그룹) 등을 생성한다. 이 과정에서 산소 소비 및 물질의 환원이 연속적으로 일어난다. 일반적으로, 용존 산소가 약 6-10 µM일 때 탈질산화(denitrification)가, 약 1.5 µM 일 때, 망간(Mn) 및 철(Fe) 수산화물이 환원된다고 알려졌다(Stumm and Morgan, 1998). 이러한 산화체(oxidants)의 존재는 일반적 미생물과 메탄 생성 미생물과의 경쟁을 유발, 메탄 생성 및 소비에 중요한 역할을 하는 것으로 알려져 있다(Lovley and Goodwin, 1988; Lovley, 1991). 즉, 메탄 생성 과정에 산소 유무가 아주 중요한 요소이고, 따라서, 산소 농도가 낮은 환경에서 메탄이 효율적으로 생성될 수 있음을 의미한다.
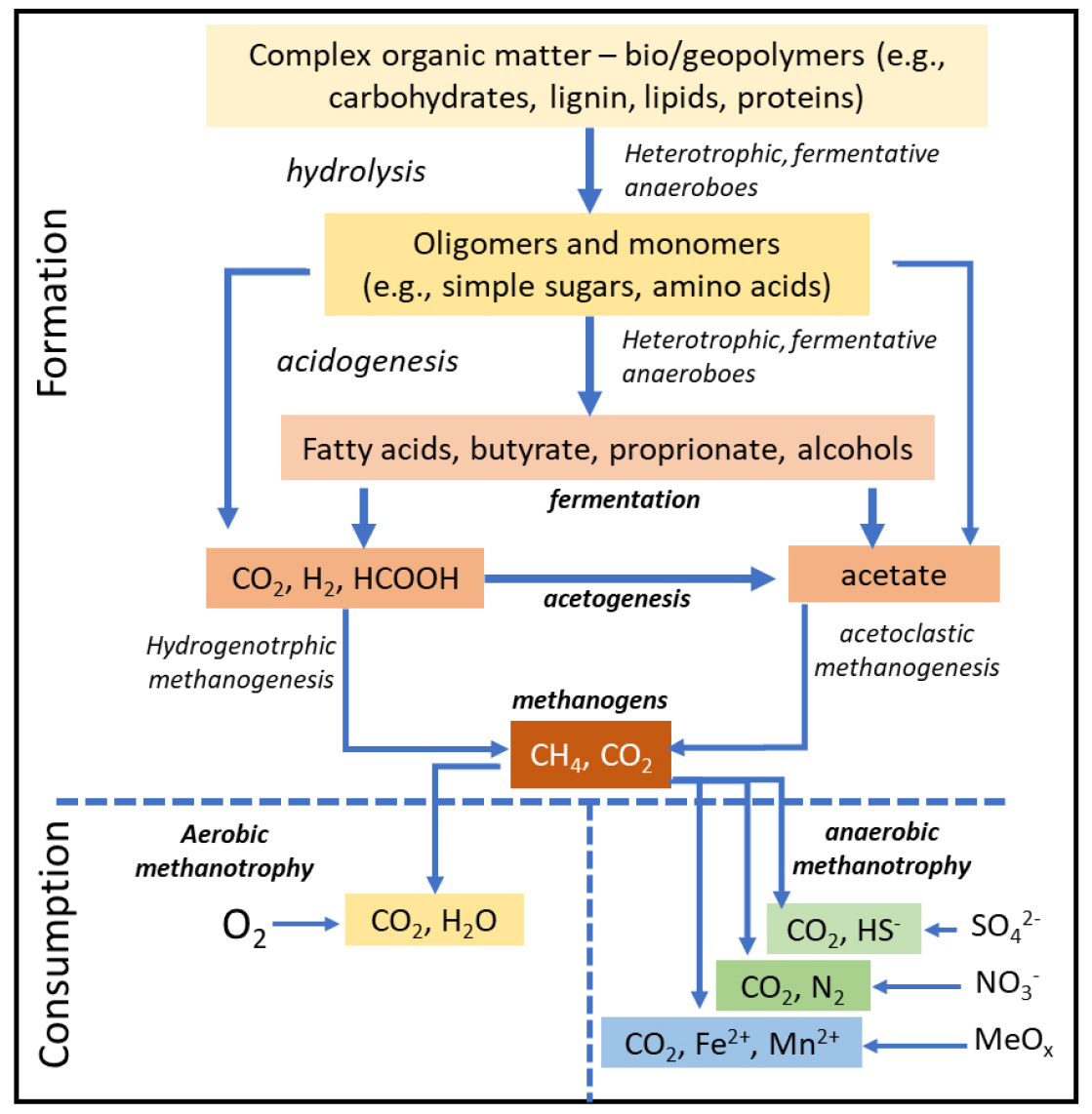
Fig. 2.
A simplified diagram for organic matter diagenesis and methane generation. This figure was modified from Whiticar(2020).
메탄 생성 과정은 화학적 변환 과정에서의 자유에너지에 따라 이루어진다. 일반적인 메탄 형성 화학식과 에너지 레벨을 Table 1에 나타냈다. 자유에너지 레벨에 따르면, CO의 환원이 가장 높은 에너지를 갖지만, 퇴적층에서 CO 농도는 아주 낮고, 이를 이용하는 미생물들은 성장 속도가 아주 느리기 때문에, 실제 메탄 생성에는 아주 미미한 역할을 하는 것으로 알려져 있다(Rother and Metcalf, 2004; Diender et al., 2015). 무기 탄소(CO2)를 이용하는 방식(즉, CO2 환원, hydrogenotrophic methanogenesis, 식 (1)) 이 가장 평범한 메탄 생성 방식이다. 두 번째 방식은(식 (2)), Acetate를 터미널 전자 수용체로 이용, 메탄과 이산화탄소를 생성하는 방식(Acetoclastic methanogenesis)이다.
이 두 방식을 통한 메탄의 생성은 일반적으로 H2-oxidizing CO2-reducting acetogenic species (Kotelnikova and Pedersen, 1998) 또는 acetate-oxidizing H2-producing anaerobes (Zinder and Koch, 1984)에 영향을 받는다. 세 번째 메탄 생성 방식은, methylotrophic methanogesis에 의해 생성되는 방식인데, 단순한(한 개의 탄소를 포함한) 탄화수소체(e.g., methanol, methylamines, and methylsulfides) 등을 메탄 생성 미생물(methanogenesis)이 이용하여 메탄을 생성한다(King et al., 1983; Oremland, 1988; Lang et al., 2015). 이러한 methylotrophic 메탄 생성 기작은, 사용하는 효소 M 또는 B에 따라, 수소-의존성 또는 수소-비의존성으로 나눠진다(Keltjens and Vogels, 1993; Sikora et al., 2017; Lackner et al., 2018). 종합해 보면, 일반적 환경에서 acetoclastic 메탄 생성이 미생물에 의해 생성된 메탄의 약 2/3 정도(약 50~90% 정도로 추정) 되는 것으로 추정하고 있다(Conrad and Klose, 1999; Le Mer and Roger, 2001; Kotsyurbenko et al., 2004; Valentine et al., 2004; Goevert and Conrad, 2009).
Table 1.
Common methanogenic substrates. Free energies (ΔG°) are at standard state and pH = 7, but ΔG° will vary in nature with actual activities of the reactants and environmental conditions. (Rother and Metcalf, 2004; Whitman et al., 2006; Liu and Whitman, 2008)
| Substrates | Representative reactions | ΔG (kJ mol-1 of CH4) |
| Carbon dioxide + hydrogen gas1 | CO2 + 4H2 CH4 + 2H2O | -131 |
| Acetate2 (acetic acid)1 + proton | CH3COO- + H+ CH4 + CO2 | -36 |
| Formate3 | 4HCOO- CH4 + 3CO2 + 2H2O | -130 |
| Methanol3 + hydrogen gas | CH3OH + H2 CH4 + H2O | -113 |
| Methanol3 (hydrogen independent) | 4CH3OH 3CH4 + CO2 + 2H2O | -105 |
| Ethanol3,4/(1-propanol3,4 and 1-butanol2,4) + carbon dioxide | 2C2H5OH + CO2 CH4 + 2CH3COO- + 2H+ | -112 |
| Carbon monoxide + water | 4CO +5H2O CH4 + 3HCO3 + 3H+ | -196 |
| Methylamine3 + water | 4CH3NH3+ + 2H2O 3CH4 + CO2 + 4NH4+ | -75 |
| Dimethylamine3 + water | 2(CH3)2NH2+ + 2H2O 3CH4 + CO2 + 2NH4+ | -73 |
| Trimethylamine3 + water | 4(CH3)3NH+ + 6H2O 9CH4 + 3CO2 + 4NH4+ | -74 |
| Dimethylsulfide3 + water | 2(CH3)2S + 2H2O 3CH4 + CO2 + H2S | -74 |
2.3 해수 내 메탄 생성(메탄 역설)
대양 상층 혼합부는 상대적으로 대기-해양 평행 농도보다는 상대적으로 높게 나타나는데, 이런 메탄 과포화는 대부분 대양에서 나타난다. 일반적으로 메탄의 형성은 산소가 극히 낮은 농도에서 발생하는데, 해양 표층은 산소 과포화 지역으로, 일반적으로 메탄 생성은 일어나지 않는다고 알려져 있다. 따라서, 해양 표층의 메탄(대기-해양 평행 값에 비해) 과포화를 “메탄 역설(methane paradox)” 라고 불리는데, 아주 오랫동안 논쟁으로 남아있다. 메탄 역설은 여러 가지 가설이 있는데, Reeburgh(2007)는 해양 표층 내 동물성 플랑크톤의 체내 내장 산소가 없는 환경에서 메탄이 생성되어 배출되기 때문일 거라고 제안하였다. 하지만, 최근 Karl et al.(2008)과 Repeta et al.(2016)은 대양 표층 빈 영양화 상태에서, 메탄-인 화합물(methylphosphonate) 이 미생물이 인을 분리/분해(decomposition)하는 과정에서 잉여물로 생성된다고 밝혔다. 또한, Perez-Coronel and Michael Beman(2022)는 단순히 methylphosphonate를 분해하는 미생물뿐만 아니라, 다른 미생물들도 메탄 생성에 기여한다고 밝혔다. 또한, 최근 Damm et al.(2010)은 북극해 표층에서 해수 내 인(P)이 풍부한 지역에서도 메탄의 농도가 대기 평형 농도보다 과포화되어 있는 것을 발견하였다. 이 지역은 인은 풍부하지만, 질소가 부족한 환경이고, 이러한 환경에서는 질소고정을 할 수 있는 종이 우점하였으며, 이런 생태계적 특징에서는 dimethylsulfoniopropionate (DMSP)가 풍부히 생성되는데, 미생물이 이 DMSP를 분해하는 과정에서, 메탄이 생성되었으리라 추측하였다. 이처럼, 해양 표층 메탄 역설에 관해 많은 가설과 약간의 연구가 진행되었을 뿐, 아직 명확하게 밝혀지지 않고 있다.
2.4 퇴적층에서 메탄 생성
퇴적층 내 메탄 생성은, 일반적으로 산화-환원 사다리(Redox ladder) 가장 바닥에 위치하며, 수층으로부터 공급된 유기물 환원으로 발생한다(Figs. 2 and 3) (Stumm and Morgan, 1998; Stigliani, 1988). 퇴적층내 산소가 없는(혹은 아주 적은) 퇴적층 및 수층에서, methanogenesis에 의해서 메탄은 생성되는데, 산소 농도(혹은 산화-환원 상태)에 따라 수 cm에서 m까지 발생한다. 일반적으로, 퇴적 표층은 저서생물 등의 교란으로, 산소가 풍부한 환경이다. 이후, 산소가 농도가 낮아지면, 질산염 및 망간/철 화합물, 이후 황화물이 환원된다. 황화물 환원 대와 메탄 생성 구간에서는 Sulphate-Methane Transition Zone (SMTZ)이 존재하는데, 이 구역에서 메탄은 황화물 환원에 전자 기여자 역할을 한다(Fig. 3). 이러한 화학적 작용으로, 메탄 농도는 급격하게 감소하게 된다(메탄 제거 부분 참조). 하지만, 깊은 퇴적층 내 메탄 농도는 표층보다 약 1000 배 이상 높기 때문에(µmol ~ mmol 수준), 적은 양이 퇴적 표층으로 확산을 통해 공급되더라도 해수보다는 높은 농도를 나타낸다. 많은 유기물이 존재하는 퇴적층에서는 메탄의 농도가 아주 높게 나타날 수도 있는데, 이때 메탄은 메탄 방울 형태로 SMTZ를 지나쳐 수층 및 대기까지 메탄 방울 형태로 유출될 수 있다.
2.5 해양 퇴적층 내 메탄 생성
해양 퇴적층 내 미생물에 의한 메탄 생성 양은 아직 명확하게 규명되지 않았지만, 일반적으로 자연발생 기작의 1/3(약 10~40%) 정도 차지하는 것으로 알려져 있다(Whiticar, 2020). 퇴적물에서 메탄 유출은, 생성 및 소비, 이동 방식(확산, 이류)에 의해 영향을 받는다. 이와 더불어, 열변형(thermogenic) 및 비생물(abiotic) 기원에 의한 메탄 유출 또한 해양 퇴적물 내 메탄 총량(budget)에 영향을 미친다(예, submarine seepages) (Etiope and Klusman, 2002). 해양 퇴적물 내 메탄 생성 양은 연간 5-300 Tg-CH4 (Reeburgh et al., 1993; Hovland et al., 1993; Hinrichs and Boetius, 2002)로 아주 광범위하게 추정되고, 최근 모델링 결과는 이보다 적은 5-33 Tg-CH4/year 로 추정하였다(Wallmann et al., 2006; Boetius and Wenzhofer, 2013). 이는 앞서 이야기한 시공간에 따른 생성 및 소비 또는 확산, 이류, 유출량 변화 때문이다. 해양 환경에서 대기로 유출되는 양은 최근 IPCC 보고서에 따르면, Top-down 방식에서는 연간 23 Tg-CH4, Bottom-up 방식은 연간 45 Tg-CH4로 추정하였다.
해양 퇴적물에서 메탄의 생성은, Jørgensen(1977)이 지적했듯이, 서로 다른 유기물 분해/환원(또는, 서로 다른 터미널 전자 수용체 존재) 구간에 따라, 메탄의 거동이 달라지는데, 예를 들어, 해양 퇴적물 내 다량의 황화물과 이에 따른 황화물 환원 미생물에 의해 메탄 생성의 초기 물질인 acetate는 메탄으로 변환되기 전에 대부분 소모되기도 한다(메탄 제거 부분 참조). 이러한 환경에서는, 수소 기반 메탄 발생이 주요 요인이 된다.
퇴적물 표층은 일반적으로 산화 환경이고, 깊이가 깊어질수록 환원 환경으로 바뀐다. 저서생물에 의한 퇴적물 변형은 퇴적물 내로 산소를 유입시켜, 퇴적층 산화-환원 환경 조건을 바꾼다. 이러한 퇴적물 변형은 깊은 층에 축적된 높은 농도의 메탄을 해수로 유출하기도 하지만(Bonaglia et al., 2014), 반대로 산소 공급을 통해 메탄을 감소시킬 수도 있다(Childress et al., 1986). 퇴적층 내 생분해성 유기물(labile organic matter) 농도가 적은 북태평양 중부 지역에서는 산소 농도가 약 250 µM 정도로 높다(Whiticar, 2020). 이러한 지역에서 유기물들은 대부분 난분해성 유기물(recalcitrant organic matter)이고, 산소를 고갈시킬 만한 충분한 유기물이 존재하지 않아 산소가 수십 미터까지 존재한다(Fig. 4). 따라서, 이 지역에서 메탄 생성은 효과적이지 않다(D’Hondt et al., 2015). Schonheit et al.(1981)와 Ragsdale and Kumar(1996)는 산소 농도가 약 10 mg/kg 일 때는 메탄 생성이 발생하지 않을 수 있고, 이는 메탄 생성 효소와 cofactor가 산소에 민감해서 작용을 못하기 때문으로 보고하였다. 반면에, 생분해성 유기물이 많은(~ 0.3 wt%) 대륙붕 환경에서는 이런 유기물들의 분해가 산소 유입 양 및 속도보다 빨라, 산소 고갈 현상이 대략 퇴적층 표면 수 mm에서 cm까지 발생한다(Fig. 4). 이렇게 산소가 고갈되면, 미생물(유기물과 산소를 소비하는)은 비교적 에너지가 작은 아산소산화물(Suboxic oxidant; nitrate, nitrite, and Fe/Mn-oxides)이, 이후 산소가 더 감소하여 무산소 환경이 되면, 용존 황화물(sulfate)이 황화물 환원 미생물(sulfate reduction bacteria; SRB)에 의해 환원된다. 흥미로운 점은 황화물 환원 구역 바닥(혹은, 메탄 생성 시작 구역)에서도 황화물은 다 사용되어 없어지지 않고, 약 수 백 µM 농도로 존재한다(Neretin et al., 2004). 즉, 이 정도 농도의 황화물이면, 대부분의 메탄은 산화되어(거의 0에 가까울 정도로) 얕은 퇴적층에서 메탄은 측정 안될 정도의 농도이어야 하지만, 이 지역에서도 메탄의 농도는 수백 nM 정도로 높게 나타난다(Whiticar, 2020). 이와 같이 유의미한 황화물이 존재함에도 메탄이 다 산화 제거되지 못한 이유는 아직 명확하게 구명되지 않았는데, 아마도 수백 µM 농도(혹은 이하)에서 황화물 환원 미생물의 활동이 제약받기 때문으로 생각된다(Leloup et al., 2007).
유기물 속성(diagenetic process)의 마지막 과정은 메탄 생성 미생물(methanogenesis)에 의한 메탄 생성이다. 일반적으로, 유기물이 많은 퇴적층은 산소 농도가 아주 낮아, 메탄이 생성되어 축적이 이루어진다. 특히, Black Sea 및 Saanich Inlet 등은 아주 좋은 예이다(Luther et al., 1991; Capelle et al., 2018). 특히, 유기물 공급이 많은 해양, 강 하구, 폐쇄성 만 등에서는 높은 농도의 메탄이(~ 10 µM) 해수층에서도 발견된다(Saanich Inlet, Lilley et al., 1982; Black Sea, Reeburgh et al., 1991; Schubert et al., 2006). 하지만, 최근 연구에 따르면, 메탄 생성이 유기물 속성 작용 중간에도 나타날 수 있다는 가능성을 제시하였다. 예를 들어, Crowe et al.(2011)은 철과 망간이 풍부한 호수(Matano, Indonesia) 수층에서 메탄 생성 미생물을 검출하였고, 이에 따라 메탄 생성 미생물이 철과 망간 수산화물을 이용해서 메탄을 생성할 수 있다는 것을 보고하였다. Lovley(2006)과 Weber et al.(2006)은 이 과정이 생물학적으로 가능할 수 있다고 제안하였다.
앞서 이야기한 산소가 부족한 환경에서 메탄 발생 과정 이외에 아주 특수한 환경에서도 메탄 발생이 일어난다. 예를 들어, Takai et al.(2008)은 온도가 아주 높은(~ 122°C) 환경에서 메탄이 생성되는 것을 보고 하였고, Kashefi and Loveley(2003) 과 Lilley et al.(1993) 열수광상(hydrothermal vent)의 높은 온도 환경에서 서식하는 메탄 생성 미생물을 발견하였다. 이와는 반대로, 아주 저온에서 자라는 메탄 생성 미생물 또한 발견되었는데, Nozhevnikova et al.(2003)은 스위스 Baldegg and Soppen 호수 약 1°C 수층에서 메탄 발생 미생물을 배양하였고, Whiticar et al.(1986)은 남극해 퇴적물 약 -1.3°C 환경에서 높은 메탄 농도를 바탕으로, 저온에서도 메탄 생성 미생물이 존재할 수 있음을 제안하였다. 이외에도 실험실 배양을 통해, Rivkina et al.(2002, 2004)는 -16.6°C 에서도 메탄 생성 미생물이 존재할 수 있음을 보였고, 여러 빙하에서도 미생물을 발견하였다(Campen et al., 2003; Price and Sowers, 2004). 또한, Takai et al.(2008)과 Zeng et al.(2009)은 높은 압력에서도 메탄 발생 미생물종을 보고하였다. 높은 염분과 pH 환경에서도 메탄 생성 미생물이 발견되었는데, Oremland et al.(1993)은 미국 Mono and Big Soda 호수의 높은 염분 40-95 g/l 와 pH 10 인 환경에서 메탄 생성 미생물이 활동하는 것을 보고 하였다. 또한, Kevbrin et al.(1997)은 케냐 Magadi 호수(염분 300g/l, pH= 7-8) 지역에서도 비슷한 미생물을 발견하였다. 이처럼, 메탄 발생 미생물은 다양한 환경 조건에서 존재한다. 하지만, 앞서 이야기한, 해양과 육상의 일반적 자연환경에 비해 그 생성량은 아주 미미하다고 알려져 있다.
2.6 담수와 육상지역에서 메탄 생성
담수와 해수의 가장 큰 차이는 황화물의 농도이다(~50 µM 담수 vs 25-30 mM 해수). 즉 황화물 환원이 해수에 비해 담수에서 아주 약하고, 따라서, 황화물 환원에 의한 메탄 제거가 효과적으로 나타나지 않는다(Ingvorsen and Jørgensen, 1984). 최근, 연구에 따르면, 전 지구적 메탄 유출량은 육상의 강이나 호수에서 약 100 Tg-CH4 year-1(Bastviken et al., 2011)인데, 해양에서 유출량은 약 10-30 Tg-CH4year-1로, 약 3배 이상 높다(IPCC 보고서, Canadell et al., 2021).
담수의 낮은 황화물 농도는, 결과적으로 황화물 환원 대(zone)가 아주 얇다는 것을 의미하고, 따라서, 담수에서 메탄 생성은 퇴적층 표층에 가까운 지역에서 발생한다. 즉 황화물이 <30 µM 인 지역에서는 수 cm 내에서 메탄이 발생할 수 있다(Kuivila et al., 1989; Koizumi et al., 2003). 하지만 황화물의 농도가 약 60 µM 이상 되는 곳에서는 황화물 환원 미생물의 활발한 활동으로 메탄 생성이 감소할 수도 있다(Lovley and Klug, 1986). 담수의 낮은 황화물과 황화물 환원 미생물 환경에서는 메탄 생성 시 사용되는(acetate 를 이용하는) acetoclastic 메탄 발생 기작이 hydrogenotrophic (H를 이용하는) 메탄 발생 기작보다 훨씬 중요하다. 몇몇 육상 무산소 호수 및 습지 지역에서, acetoclastic 메탄 발생 기작은 퇴적물 표층에서, hydrogenetrophic메탄 발생 기작은 퇴적물 깊은 층에서 주요한 메탄 발생 기작으로 알려져 있다(Whiticar, 2020). 이러한 수직적 주요(primary) 발생 기작 변화는 acetoclastic 메탄 발생에 이용되는 유기물의 여부에 따라 다르게 나타난다고 알려져 있다(Whiticar, 2020). 호수 퇴적층에서, 용존 메탄 농도가 쉽게 과포화 되는데, 몇몇 경우에는 방울이 형성 및 호수 표면으로 방출된다.
육상환경에서, 혹은 수심이 낮은 연안 환경, 염습지 등에서 메탄의 대기 유출은 확산 및 기체 방울로 유출과 더불어 식물에 의한 유출이 아주 중요하다. 일반적으로, 메탄의 공기 중 확산 속도는 2.0 * 10-1 cm2 s-1 로 물을 통과하는 확산 2.0 * 10-5 cm2 s-1 보다 아주 빠르다(Whiticar, 2020). 즉, 식물을 통한 대기로 직접 유출이 토양이나 수층을 통과하는 확산보다 휠씬 용이하고 효과적일 수 있다. 예를 들어, Tyler et al.(1997)은 Texas paddy 지역에서 발생하는 메탄 방출의 약 98%가 식물에 의한 것으로 보고 하였고, Watanabe et al.(1999)는 쌀 재배 지역에서 메탄 유출량의 약 60%가 벼의 뿌리와 잎을 통해 대기로 직접 유출된다고 밝혔다. 또한, 식물 뿌리 산출물(Root exudates)이 이탄지대(peatland) 와 북극 습지 메탄 생성에 아주 중요한 역할을 하는 것으로 보고 되었다(Shannon et al., 1996; Ström et al., 2012). 유사하게, Knoblauch et al.(2015)는 북극 Siberia 지역 툰드라 지역에서, 총 메탄 유출량의 70-90%가 식물을 통하여 이루어졌을 것으로 추정하였다.
벼 외 다른 식물 또한 메탄 수송 통로로 잘 알려져 있다. 예를 들어, Colmer(2003) 과 Chanton(2005)는 macrophytes의 동맥엽(aerenchyma)을 통한 메탄 유출을 보고 하였고, Terazawa et al.(2007)은 범람원(floodplain) 숲에서 대기 중 메탄 유출이 식물 체내 공간을 통해 이루어졌을 것으로 판단하였다. 또한, 메탄은 고지대 나무 등에서 아주 높은 농도로 축적될 수 있고(Mukhin and Voronin, 2007; Covey et al., 2012; Hietala et al., 2015), 몇몇 경우, 대기로 방출되는 양은 토양으로 유입되는(혹은 토양에서 생성되는) 메탄 양의 약 30-90%(평균 63%) 정도 되는 것으로 알려져 있다(Wang et al., 2016). 이와는 반대로, 식물은 또한 중요한 메탄 소비자이다. Schütz et al.(1989), Groot et al.(2003), 및 Zhang et al.(2014)은 벼 재배 지역 내 식물 근권(rhizosphere) 산소가 있는 환경에서 메탄이 소비된다고 밝혔다.
3. 메탄 제거
생물 및 무생물에 의한 메탄 산화는 퇴적층, 토양, 물, 및 대기에서 아주 중요한 메탄 제거 방식이다. 대기에서 메탄 산화는 복잡한 광화학적 과정을 거친다. 즉, 활성수산화물(hydroxyl radical)이 메틸과 메틸-과산화물, 메탄올, 일산화탄소를 거쳐 이산화탄소로 산화된다.
이 활성수산화물 반응(OH radical abstraction reaction)은 대류권에서 메탄의 주요 제거 방식이고, 이 방식으로 연간 약 430 Tg-CH4 제거된다(Khalil and Rasmussen, 1983; Crutzen, 1991; Whiticar and Schaefer, 2007). 이와 더불어, 대기에서 중요한 메탄 제거 기작은 토양 미생물에 의한 제거(약 25-40 Tg-CH4 year) (Seller and Conrad, 1987; Conrad, 1996; Topp and Pattey, 1997), 성층권 제거 ~ 40 Tg-CH4 year (Boucher et al., 2009), 해양과 대기 경계면에서 염소(Chlorine)와 반응하여 제거 ~ 30 Tg-CH4 year (Wang et al., 2002; Allan et al., 2005, 2007)이다.
3.1 유산소 메탄 제거(Aerobic methane oxidation)
생물에 의한 메탄 산화는 유 및 무산소 환경에서 발생한다. 메탄 산화에 관한 다양한 반응식과 에너지는 Table 2에 나타냈다. 메탄 산화 미생물은 메탄을 탄소원으로 사용하여, 수소 제거 과정을 통해 중간체인 메탄올(methanol), 폼알데하이드(formaldehyde), 포메이트(formate)를 통해 궁극적으로 이산화탄소로 변환한다. 메탄 발생 미생물들은 일반적으로 단지 메틸만을 이용하여 생존하는것(Methylotrophs)으로 알려져 있었으나, 몇몇 종은(예, Methylocystis, Methylocella spp.) 메틸뿐만 아니라, 메탄, 에탄, 및 acetate 등도 이용하여 성장하는 것으로 알려져 있다(Im et al., 2011). 가장 기본적인 유산소 메탄 산화 방식은 아래(식 (4))와 같이 나타낼 수 있다(Dalal and Allen, 2008).
일반적으로, 메탄 산화 미생물은 메탄을 이용할 수 있는 효소 methane monogeneses (MMO) 생성 여부에 따라 두 그룹으로 나뉘는데, 세포막에 흡착된 입자 형태로 구리(Cu)를 필요로 한 pMMO와 용해된 상태로 철(Fe)이 필요한 sMMO로 나뉜다(Ghashghavi et al., 2017). 따라서, 미량원소(Fe, Cu, Co, Mo) 가 부족한 해양 환경에서는 유산소 메탄 제거가 효과적이지 않을 수 있다(Glass and Orphan, 2012). 최근, Shiller et al.(2017)은 배양 및 현장 실험을 통해, 희토류 원소(La, Ce)가 메탄 제거에 아주 중요한 역할을 하는 것을 밝히기도 하였다. 메탄 제거 미생물 속(methanogrophic genera)에는 현재까지 3 집합체로 구분되는데, Ribulose monophosphate (RuMP)를 거치는TYPE I(예, Methylobacter와 Methylomonas), serine 과정을 거치는 TYPE II(예, Methlosinus, Methlocella와 Methylocystis), 그리고 위 두 과정을 동시에 거치는 TYPE X(예, Methylococcus capsulatus) 으로 나뉜다(Hanson and Hanson, 1996; Fei et al., 2014).
Table 2.
Energetics of selected diagenetic reactions for organic matter remineralization and methane oxidation in marine sediments. (From Zinder, 1993; Schink, 1997; Thauer, 1998; Amend and Shock, 2001; Whitman et al., 2006; Deutzmann and Schink, 2011; Ferry, 2011)
유산소 환경 메탄 산화는 탈질산화 과정과 밀접하게 연관되어 있다. 즉, monooxygenases (MMO)와 암모니아 MMO와 유사하게, 많은 methane oxidizing bacteria (MOB)는 산소가 적은 환경에서 N2를 만들 수 있다. Zhu et al.(2016)는 유산소 메탄 산화와 탈질산화 과정의 궁극적인 화학 양론적(stoichiometric) 방정식을
로 제안하였다.
몇몇 경우에, 메탄 산화 미생물은 극한 환경에서도 생존 가능한데, 예를 들어 높은 온도(62°C, Bodrossy et al.(1995), 초저온(4°C, Omelchenko et al., 1996; Wartiainen et al., 2006), 산성(pH 5.0, Dedysh et al., 2000), 알칼리 환경(pH 10, Sorokin et al., 2000), 및 고염분(5.6%, Fuse et al., 1998; Kalyuzhnaya et al., 2008)에서 메탄 산화 미생물의 성장이 보고 되었다.
토양 내(유산소) 메탄 제거 미생물은 메탄 농도(혹은 포화도, Km)에 따라 “낮은(Low-)” 혹은 “높은(High-) 친화도(Affinity)”로 구분되며, 일반적으로 Km이 µM 수준이면, “낮은 친화도”, nM 수준이면 “높은 친화도”로 구분하고 있다(Bender and Conrad, 1992). 이러한 메탄 친화도의 높고 낮음에 따라 최고 산화율(maximum oxidation rate; Vmax) 및 임계 농도(threshold mixing ratio; Tha)가 다르게 나타나는데(Nayak et al., 2007; Conrad, 2009), 낮은 친화도 미생물은 전형적으로 높은 Km, Vmax, 및 Tha 값을 갖는다(Bender and Conrad, 1992). 높은 친화도 미생물은 낮은 Km, Vmax, 및 Tha 계수 값을 갖으며, 대기중 메탄이 땅(건조한 땅)으로 확산(혹은 평형) 되는 농도와 같이 낮은 메탄 농도 환경과 관련 깊다(일반적으로 대기 메탄을 산화시키는 주요한 역할을 한다) (Bender and Conrad, 1992; Dunfield et al., 1999; Dunfield and Conrad, 2000). 일반적으로 “낮은 친화도”에서 활동하는 미생물은 높은 메탄 농도 환경(유기물이 풍부한 토양, 툰드라 토양, 매립지 등)에 존재하며, 전통적으로 Type I에 해당하는 미생물을 일컫는다. “높은 친화도” 미생물은 메탄 농도가 낮은(대기-토양 평형 농도) 환경에서 발견되는 미생물을 일컫는다(Bender and Conrad, 1992; Nayak et al., 2007). 특히, TYPE II 미생물은(예, Methylocystis) 전형적으로 낮은 메탄 농도 환경에서 우점하는 종이라고 알려져 있고, 이러한 미생물은 토양, 숲 및 호수 등에서 대기(대류권) 중 연간 메탄 총제거량 480 Tg-CH4의 약 5~8%를 차지하는 등 아주 중요한 역할을 하는 것으로 알려져 있다(Benstead and King, 1997; Henckel et al., 2000). 이러한 TYPE II 방식의 메탄 제거는 메탄 및 산소 농도, 온도, 토양 수분율, 및 pH 등에 따라 큰 영향을 받는다(Oertel et al., 2016). 일반적으로 호수에서, 유산소 메탄 산화는 메탄 유출을 조절하는 데 아주 중요한 역할을 하고, 이러한 유산소 메탄 제거 미생물은 생성된 메탄의 30~99%를 제거하는 것으로 알려져 있다(Bastviken et al., 2008). 전지구적 담수로부터 발생하는 메탄은 연간 약 ~ 100 Tg-CH4로 알려져 있는데(Bastviken et al., 2011), 고산지대 툰드라 에서는 연간 약 35 Tg-CH4라고 알려져 있다(Fung et al., 1991).
여러 연구에 따르면, 메탄은 온대 지역 토양에서 열대 지역 토양보다 더 많이 제거되는 것으로 알려져 있고, 활엽수 지역 토양에서 침엽수 지역 토양보다 더 많이 제거되는 것으로 알려져 있다(Meyer et al., 1997). 또한, 토양의 수분이 많고, 조직과 압축 정도가 낮아 산소 투과율이 높은 지역, 유기물이 많은 토양, 교반이 덜 되어 있는 토양에서 메탄이 더욱더 효과적으로 제거되는 것으로 나타났다(Boeckx et al., 1997; Del Grosso et al., 2000; Templeton et al., 2006; Abushammala et al., 2014).
종합해 보면, 유산소 메탄 산화는 담수 및 해수에서 모두 발생한다. 일반적으로 이런 산화는 약 연간 10-200 pM 정도로 낮다고 알려졌지만(Scranton and Brewer, 1977; Rehder et al., 1999; Grant and Whiticar, 2002; Reeburgh, 2007), 수층 및 퇴적층 무산소 환원 환경에서 해수 상층 및 대기 유산소 층으로 유입되는 메탄의 거동과 대기로의 유출을 줄이는 데 유의미한 역할을 하는 것으로 알려져 있다(Grant and Whiticar, 2002).
3.2 무산소 메탄 산화(Anaerobic methane oxidation)
무산소 메탄 산화는 대부분 무산소 해양 퇴적물에서 발생하며, 보통 황화물-메탄 전환 지역(Sulfate-methane transition zone; SMTZ)에서 발생한다. 그러나, 실제 과정은 아직 명확하게 알려지지 않았다. 해양 퇴적층 무산소 메탄 산화는 연간 70~300 Tg CH4 메탄을 제거하는 것으로 알려져 있다(Reeburg, 1996; Hinrichs and Boetius, 2002; Boetius and Wenzhöfer, 2013). 무산소 메탄 산화는 해양 퇴적층에서 발생하는 메탄 생성의 약 75~95% 정도에 달하는 것으로 알려져 있고(Valentine, 2002), 이는 해양 퇴적층 메탄 유출량인 5-33 Tg-CH4 year (Wallmann et al., 2012) 보다 큰 것으로 나타났다. 이러한 생성량보다 큰 무산소 메탄 산화는 해양에서 발생하는 지질적 유출(Seeps와 gas-hydrates)에 따른 추가적 산화에 의한 것으로 여겨진다(Whiticar, 2020). 일반적으로 퇴적물에서 수층으로 유출되는 메탄의 양은 생성량의 약 5~25% 정도로 알려져 있는데, 대부분은 유산소 메탄 산화로 인해 제거된다. 무산소 메탄 산화율은 약 1 ~ 3,000 nM(또는 연간 ~ 11 mol/m2)로 환경에 따라 아주 다양하게 나타난다(Hinrichs and Boetius, 2002; Luff et al., 2005; Regnier et al., 2011). 최근 연구결과, 미국 Gulf of Mexico와 해령(ridge)의 깊은 수심에서 하이드레이트 메탄이 용출되는 곳에서 높은 무산소 산화 및 황화물 환원에 따라 메탄 용출이 크게 영향을 받는 것으로 나타났다(Torres et al., 2002; Joye et al., 2004).
용존 황화물 환원(Sulfate Reduction)에 따른 메탄 산화(제거)는, 총 메탄 산화에 아주 큰 역할을 하는데, 일반적으로 다른 전자 수용체(O2, NO3-, Mn(IV)와 Fe(III)) 보다 약 50-100 배 정도 효과적이라고 알려져 있다. 유기물이 풍부한 환경에서, 용존 황화물은 황화물-환원 구역에서 상층 퇴적물과 해수에서 유입되는 속도보다 훨씬 빠르게 제거(또는 환원)된다(Figs. 4 and 5). 이 황화물-환원 구역에서 메탄의 농도는 아주 적고, 이 구역 밑에서 메탄은(특수한 경우 메탄 방울을 형성할 정도) 축적되기 시작한다. 이러한 유기물(혹은 산화-환원 사다리) 속성(diagenesis)에 따른 용존 황화물과 메탄 형성 깊이 변화는(혹은 깊이에 따른 황화물과 메탄의 분포) 황화물 환원 미생물(SRBs)과 메탄 생성 미생물과의 경쟁에 의한 것으로 설명할 수 있는데, 일반적으로 황화물 환원 미생물이 용존 황화물 구역에서 메탄 생성 미생물에 대해 우점하기 때문으로 알려져 있다. 다른 관점으로, 황화물이 환원되는 구역에서 메탄 생성 전 물질(예, acetate)이 적게 존재하고, 메탄 산화 미생물이 생성 미생물보다 훨씬 많이 존재하기 때문으로 볼 수 있다. 예를 들어, Cappenberg(1975)는 S2-가 메탄 생성 미생물의 성장을 저하시키기 때문에, 황화물 환원 구역에서 메탄의 축적이 이루어지지 않는다고 보고하였다. 이러한 설명은 깊이에 따른 메탄 농도 분포를(황화물 환원대에서 메탄 농도가 줄어드는) 기반으로 한 설명이다. 하지만, 이 황화물 환원대 밑에 축적된 메탄 농도(~ mM 수준)와 이러한 농도 구배에서 발생하는 전형적인 확산 등을 고려할 때, 메탄 농도 변화는 좀 더 천천히 줄어드는 경향을 보여야 한다(Whiticar, 1978). 따라서, SMTZ에서 실제 발견되는 급격한 농도 변화는 이 구역 내에 메탄을 소비하는 미생물이 있음을 의미한다(Whiticar, 1978). 이후, 다양한 미생물에 관한 연구로 이 황화물 환원대에서 메탄을 제거하는 미생물이 존재함을 밝혔다(Valentine and Reeburgh, 2000; Hinrichs and Boetius, 2002; Valentine, 2002).
무산소 메탄 산화와 황화물 환원을 결합하는 전통적 설명은 황화물 환원 미생물과 메탄 산화 미생물 간의 Syntrophic(한 미생물의 대사 활동 부산물이 다른 미생물의 대사를 촉진하는) 작용을 의미한다(Alperin and Reeburgh, 1985; Boetius et al., 2000; Valentine 2002; Orcutt et al., 2008). 이와 같은 화학량 적 반응식은
로 나타낼 수 있다.
Beal et al.(2009)는 무산소 메탄 산화가 MnO2와 Fe(OH)3의 환원 과정에서도 발생할 수 있음을 보고 하였는데, 이 과정은 아래 반응식으로 표시할 수 있다.
Fe/Mn 산화물과 더불어, 질산염 및 아질산염 또한 무산소 메탄 산화 반응의 전자 수용체가 될 수 있다. Raghoebarsing et al.(2006)은 미생물에 의한 탈질산화 과정에서 메탄 산화가 발생할 수 있다고 보고하였다.
라고, 제안하였다.
Raghoebarsing et al.(2006)은 담수를 이용한 무산소 환경 실험에서, 무산소 메탄 산화가 오직 탈질산화 과정에 의한 것임을 확인하였다. 이와 유사하게, Hu et al.(2015)는 무산소 암모늄 산화(anammox) 시, 메탄이 산화될 수 있음을 밝혔다.
담수에서는 해양과는 다르게 용존 황화물이 아주 적게 분포한다. 이런 환경에서는 황화물 환원에 따른 메탄 산화가 적게 나타난다(Smemo and Yavitt, 2011). 하지만, 부영양화 상태의 호수 및 강에는 황화물이 비교적 높게 나타날 수 있고, 이러한 환경에서는 황화물 환원에 의한 메탄 산화가 발생할 수 있다. 예를 들어, Cadagno 호수에서 SO42-의 높은 농도(약 > 500 uM 이상)로 인해 황화물 환원에 의한 메탄 제거가 발생한다(Schubert et al., 2011). 하지만, 황화물의 농도가 적은 지역에서는, NO2-, NO3- 등의 탈질산화 과정 및 Fe/Mn 산화물의 환원 과정에서 메탄 제거가 주로 일어난다(Sivan et al., 2011; Nordi et al., 2013). 또한, 유기산(예, 휴믹산, 또는 이와 유산한 물질) 등을 통한 무산소 메탄 제거가 중요한 제거 과정으로도 알려져 있다(Scheller et al., 2016; Reed et al., 2017).
현재까지 무산소 메탄 산화 미생물은 종 단위로 분류되기보다는 집합체(consortium of organisms)가 메탄 산화와 황화물 환원의 주체로 보고 되고 있다(Whiticar, 2020). 이는 계통발생학 적(phylogenetic) 연구와 안정/방사성 동위원소 및 분자생물학적 지시자(molecular biomarker, 예, DNA)를 이용한 연구 등을 통해 확인되고 있다. 하지만, 무산소 메탄 산화 미생물을 분리하는 연구는 syntrophic 미생물과 다양한 터미널 전자수용체 등이 관련돼 있어 아주 복잡하다(Whiticar, 2020).
4. 해양 저산소층 발달과 메탄 생성
저층수 내 산소가 풍부할 때는, 퇴적층 내 다양한 전자 수용체가 존재하여, 앞서 이야기한 자유에너지에 따라 유기물은 순차적으로 환원한다. 이 과정에서, 깊은 퇴적층으로부터 공급된 메탄이 전자 기부자가 되기도 해서, 퇴적층 내에서 대부분의 메탄은 산화된다(Fig. 3). 하지만, 저산소층이 해양 저층에 형성되면, 이러한 산화-환원 대가 퇴적층 내 아주 얕은 곳에 있거나 혹은 수층 내에 존재하게 된다. 특히, 이러한 경우, SMTZ 가 얕은 곳에 있거나 구역의 크기가 얇아질 수 있다(Fig. 5). 따라서, 퇴적층 내 메탄 산화가 효과적으로 나타나지 않아, 수층 및 대기로 보다 많은 메탄을 방출시킬 수 있다. 예를 들어, 미국의 Chesapeake 만에서, 저산소층이 발생한 여름 시기 저층의 메탄 농도가 약 40 µM로 저산소층이 발생하지 않은 시기의 메탄 농도인 약 1 µM에 비해 약 40 배 이상 높게 나타났다(Gelesh et al., 2016). 같은 시기에 표층의 농도 또한 아주 높게 나타났는데, 저산소층이 비교적 약하게 나타난 6월에 표층 메탄 농도는 약 27~68 nM이었다가, 저산소층이 강하게 나타난 9월에는 표층 메탄 농도가 약 400 nM로 높아졌다. 또한 저층수 메탄 농도는, 저/무산소층(<4.5 µM O2)이 점 차 발달하는 초기에 약 0.1 µM 에서 약 40.7 µM로 증가하였고, 무산소층이 강하게 형성된 8월 말에는 약 0.4 µM로 줄어드는 경향을 보였다(Gelesh et al., 2016). 이런 저층 메탄 농도 변화는, 퇴적층으로부터의 유입에 의한 증가와 이후 무산소 시기 수층 내 메탄 산화에 따른 것으로 보고 하였다(Gelesh et al., 2016). 이처럼, 해저 저/무산소층 시기 표층의 메탄 농도는, 많은 양의 메탄이 퇴적층 혹은 수층에서 생산되어 표층으로 유입된 것을 의미하며, 이는 많은 양의 메탄이 대기로 유출됨을 알려준다. 더 나아가, Chesapeake 전체로 확대하여 메탄의 대기 유출 총량을 추정한 결과, 하루에 약 0.8 µM이 대기로 유출된다고 가정했을 때, 저/무산소층이 형성된 시기가 약 53일 이므로, 만의 전체 넓이 11,801 km2를 고려하면, 총 ~ 19 Tg의 메탄이 유출될 것으로 추정하였다(Gelesh et al., 2016). 이 값은, 전세계적 해양-대기 메탄 유출량인 2.6 Tg 보다 높게 추정된 값인데, 한 시기의(아마도 메탄 농도가 아주 높은 시기) 값과 모든 저층에서 농도가 같을 것이라는 가정하에 추정하였기 때문으로 생각된다. 하지만, 이런 과 추정(over-estimation)에도 불구하고, 이 연구는 해양 저/무산소층이 메탄 대기 유출에 아주 중요한 역할을 한다는 것을 알려준다.
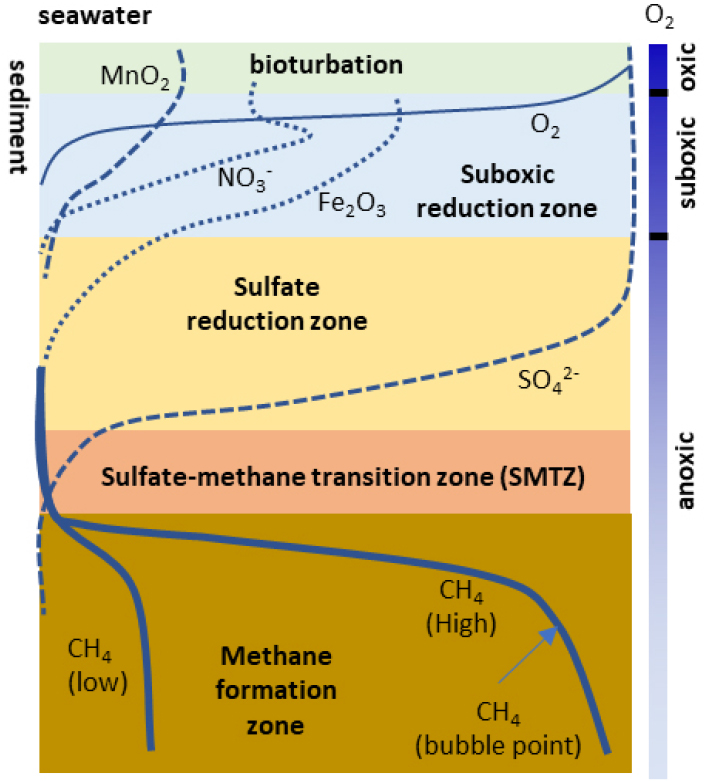
Fig. 3.
A diagram of redox conditions and terminal electron acceptors (TEA) in marine sediments. This figure was modified from Whiticar(2020).
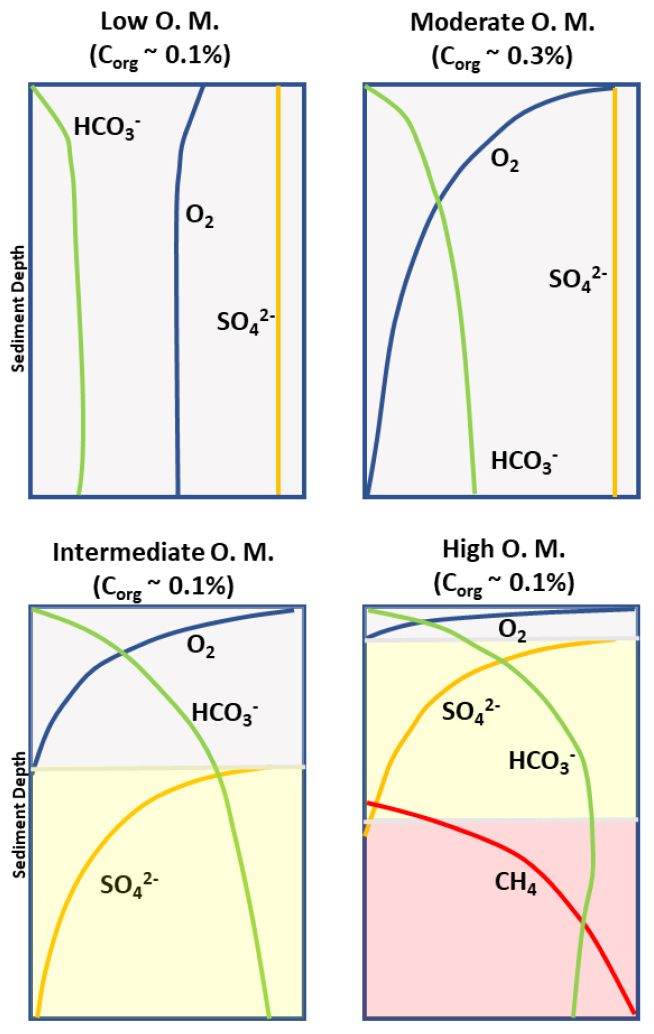
Fig. 4.
Schematic diagrams of redox species with depth and organic content in marine sediments. This figure was modified from Whiticar(2020).
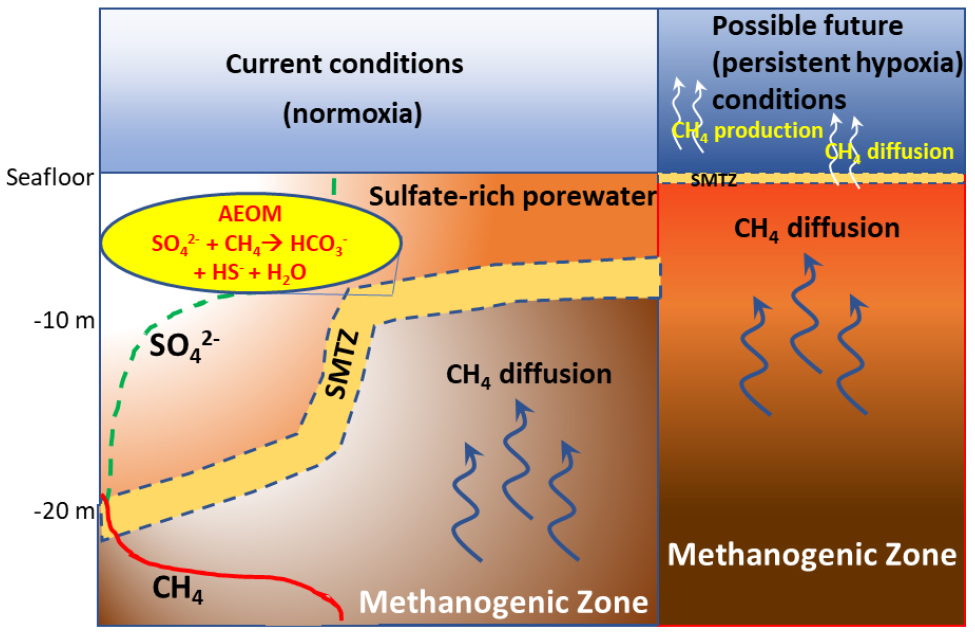
Fig. 5.
A schematic diagram showing diffusive fluxes of methane through the sulfate-methane transition zone (SMTZ) in conditions of oxic- and sub (or an-)oxic marine sediments. This figure was modified from Argentino et al.(2021).
4.1 한국 내 해수 저산소층 분포
전세계 연안 해역이 저/무산소층을 경험하고 있고(Fig. 6), 미래에는 이런 환경변화가 더욱 가속화될 것으로 예상하고 있다. 한국 연안 해역의 저산소층 발달 현황은 최근 Lee et al.(2018)과 Lim et al.(2006, 2018)에 의해 종합적이고 자세하게 연구되었다. 이들 논문에 따르면, 한국 연안 해역도 마찬가지로, 연안 해역 저/무산소층 발달이 더욱 가속화되고 있다. 특히, 한국은 만이 많고, 주변의 산업단지 및 농업 활동 지역이 많아, 해양 저산소층이 갈 수록 더욱 심해질 전망이다. 하지만, 한국 해안 저산소층 분포는 아직 연구가 미흡하다. 최근 Lim et al.(2006)과 Lee et al.(2018) 등은 한국 연안에서 기존에 시행되었던 연구들을 중심으로 강 하구 및 만 등에 저산소층 분포를 조사하였다. 이에 따르면, 한국 연안 어떤 곳보다도, 진해만의 저산소층이 가장 심하게 나타나는데, 1974년 9월에 저산소층이 최초 보고 되었으며, 이후 매년 여름이면 다시 발생하는 것으로 보고되고 있다. 이뿐만 아니라, 천수만, 가막만, 영산강 하구역, 시화만 등에서도 저산소층이 보고되고 있다.
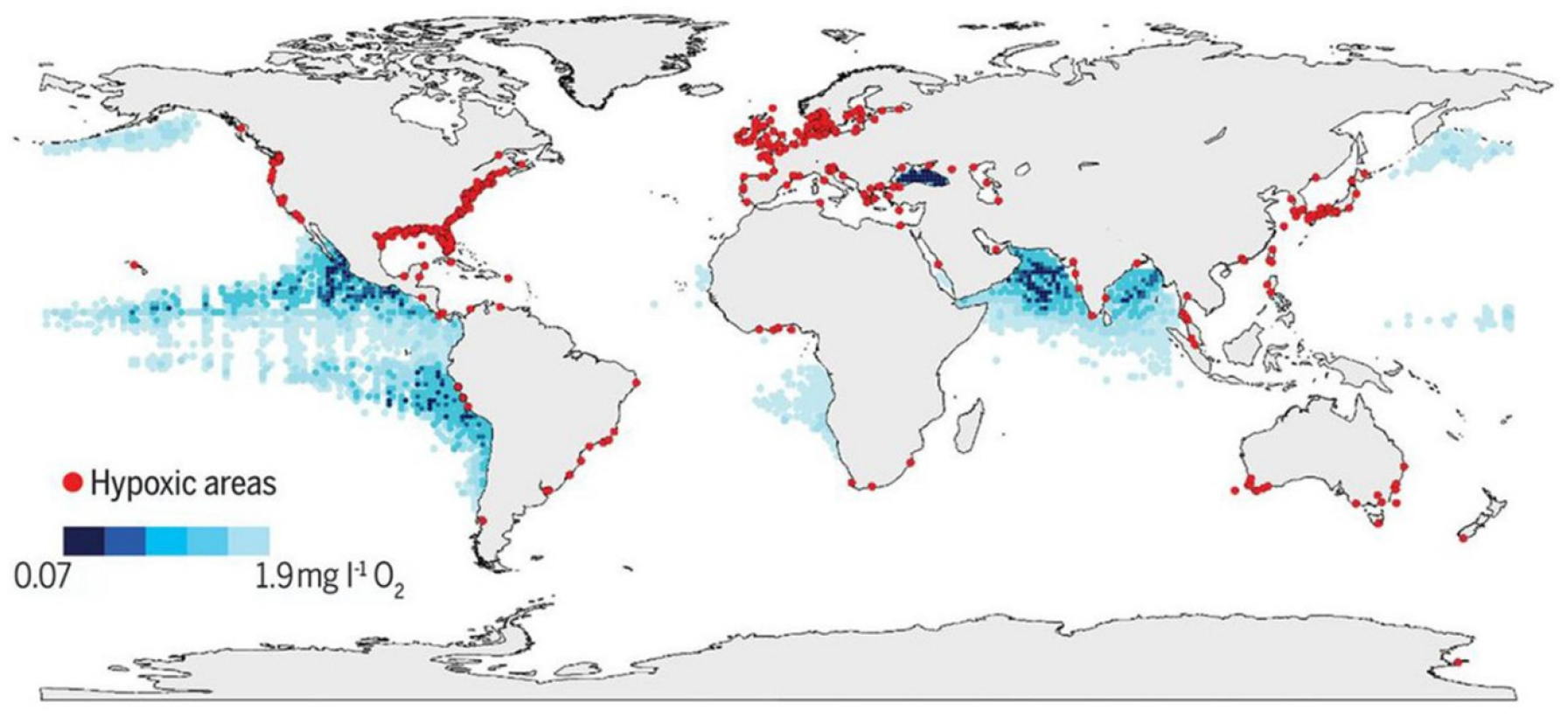
Fig. 6.
A global map of low oxygen level (< 2 mg/l) in coastal (red dots) and open oceans (blue shaded regions). This figure was taken from Breitburg et al.(2018).
진해만은 여러 다른 만(bay)들로 이루어져 있고, 가덕해를 통해 외양수가 유입, 만 안에서 혼합이 이루어진다(Kim et al., 2016). 이러한 지정학적 특징으로, 해류의 흐름이 아주 느린데, 특히 저층수의 흐름은 약 4~10 cm/s 로 아주 약하다(Kim et al., 2016). 진해만은 산업화/도시화 및 주변 농업 활동 등 인공적 영향으로 많은 종류의 영양염 등이 일일 평균 약 7,000 kg 유입되는 것으로 추정되고 있다(Lee et al., 2018). 진해만은 일반적으로 매년 5월과 9월 사이에 저산소층이 가장 강하게 형성되는데, 이 시기에는 높은 해수 표층 온도와 더불어 주위 작은 천(stream) 등을 통해 담수가 유입, 해수의 밀도 구배가 강하게 형성됨에 따라 대기-해양 기체 교환이 약화된다. 이러한 물리적 특징과 함께 풍부한 영양염 공급으로 생물 생산력이 높아져 많은 유기물이 해저에 축적되고, 이와 함께 미생물에 의한 산소 소비량이 유입량 보다 급격하게 늘어나 저산소층이 발생한다. 겨울 동안 진해만 저층 산소 농도는 약 10 mg/l로 높게 나타나다가, 3월에서 5월까지 약 2 mg/l 로 낮아진다. 여름 시기 저층 산소 농도는 2 mg/l보다 낮은 농도로 유지되다가, 가을에 2 mg/l에서 약 6 mg/l로 높아지는데, 이는 해수 온도 저하 및 바람에 의한 수직 혼합 등에 의한 것으로 알려져 있다. 진해만 여름철 저산소층은 1989년에 약 197 km2, 1993년에는 약 210 km2, 2010년에는 약 272 km2로 갈수록 넓어지고 있다(Kim and Lee, 1994; Lim et al., 2006; Kim et al., 2012; Lee et al., 2018; Lee et al., 2021). 현재 진행 중인 전 지구적 온도 상승으로 인해, 진해만의 저산소층은 더욱 넓어질 것으로 예상된다. 진해만은 큰 강의 유입이 없어, 세계 다른 지역에 비해 강으로부터 유입되는 영양염이 비교적 적지만, 다수의 양식장 등으로부터 많은 유기물과 영양염이 공급될 수 있다(예, Chen et al., 2023).
한국 연안의 특징 중 하나는, 농지(혹은 공업지) 확보를 위해 많은 지역이 인공 구조물로 연안을 연결하는 방조제(dyke)가 건설돼 있다는 것이다. 시화 및 새만금 등 많은 대규모 방조제를 비롯하여, 작은 방조제까지 합치면 2021년 기준 전국에 1,682개로 면적은 약 235,000(ha) 이다(KOSIS, 2021). 시화호는 약 13 km의 방조제가 건설돼, 약 173 km2의 육지와 인공호수가 형성되었다. 하지만, 주위 도시(안산, 시흥, 화성 등)에서 유입되는 도시 하수 등을 통한 다량의 영양염 유입과 방조제로 인한 해수 유출입 저하, 이에 따른 인공호수 내 흐름 제약으로 호수가 급격히 부영양화가 발생한다(Lee et al., 2018). 이후, 수질 관리 일환으로, 관문을 통해 해수 유출입을 가능하게 함으로써, 오염은 많이 줄어들었으나, 아직 적조 및 저산소층 형성 등의 문제가 발생하고 있다.
다른 지역의 저산소층 형성과 마찬가지로, 인공 호수내 저산소층은 여름에 발생하는데, 사화호 또한, 주변 지역에서의 과도한 영양염 유입, 해류 흐름 및 강한 밀도 구배의 동시적 작용으로 저산소층이 발생한다. 보통, 봄까지는 저층수 산소 농도는 약 8~14 mg/l로 나타나고, 여름에 호수 중앙부 저층 산소 농도는 산소 포화도의 약 10% 미만으로 저산소층이 아주 강하게 형성된다(Lee et al., 2018). 이 저산소층은 가을에 해소되는데, 이는 수온 감소와 바람의 영향으로 호수내 수직 혼합이 잘 되기 때문으로 알려졌다. 최근 조력발전소의 건설로, 시화호의 내외부 해수 이동량은 급격히 늘었으며, 이에 따라, 저층수의 산소농도는 포화도의 52% (3~154%)에서 약 95% (55~150%)로 개선되었다고 보고 되었다. 최근, Ra et al.(2013)는 시화호 내측 저층에서 여름(7월) 시기 산소포화도는 약 35%에 머무른 것을 보고하였다. Kim and Kim(2020)은 2016년 시화호 내 용존 산소가 약 4.7 ~ 8.39 mg/l였고, 8월에 가장 낮았다고 보고 하였다. 따라서, 보통 저산소층이 가장 잘 형성되는 6~7월 저층수 산소 농도는 이보다 낮을 수 있다는 가능성을 제시한다. 새만금의 경우도 최근 Kwak et al.(2023) 연구에 따르면, 여름 호수 저층 용존 산소 농도는 배수 갑문의 개폐 상황에 따라, 아주 민감하게 반응하는데, 갑문이 닫혀 물의 흐름이 약해졌을 때, 최소 2주 이상 동안, 용존 산소 농도는 2.0 mg/L 이하로 나타났다고 보고하였다. 현재, 한국의 여러 연안 환경 및 육상 강에서 수층 저산소층 발달이 진행되고 있고, 앞으로 더욱 가속화될 것으로 예상된다. 따라서, 저산소층 발달에 따른 메탄(또는 다른 온실기체) 발생 및 대기 유출이 예상되며, 그 유출량은 더욱 커질 것으로 예상된다.
4.2 진해 당동만의 성층과 빈산소에 따른 퇴적물내 혐기층 발달과 메탄
최근 Kim and An(2022)은 진해 당동만에서 해수 저산소층에서 메탄 거동을 조사하였다. 이 연구에서, 퇴적층 내 황화수소 최댓값이 저산소층 발달 전에는 약 6 cm 깊이에서 발견되었다가, 저산소 시기에는 약 2.4 cm 깊이로 상승하였음을 발견하였다. 특이하게 수층 저산소가 해소된 11월에도 퇴적층 내 황화수소 최댓값이 3 cm 깊이에서 발견돼, 저산소 지역 내 퇴적층에서는 더욱 오랜 기간 동안 메탄이 수층으로 유입될 수 있다는 가능성을 발견하였다. 메탄의 퇴적-수층 간 용출률 또한, 저산소 발생 시기 이전에 6 µmol m-2 day-1에서 저산소 시 약 1900 µmol m-2 d-1로 약 300배 이상의 증가를 보였고, 이는 황화수소 변화와 마찬가지로 수층 저산소 발생에 따른 변동이라고 보고하였다. 더 나아가, Kim and An(2022)은 진해만에서 대기로 유출되는 메탄 양을 추정하였는데, 조사 시기 메탄의 대기 유출량은 약 110-420 µmol m-2 d-1 였고, 저산소층 발생 시기에 최대 420 µmol m-2 d-1 였다고 보고하였다. 이는, 진해만을 비롯한 한국의 여러 저산소층 발달 해역에서 대기 메탄 분포에 아주 큰 영향을 줄 것으로 여겨진다.
메탄의 수층 및 퇴적층 내 생지화학적 거동을 Fig. 7에 간략하게 나타냈다. 메탄은 이산화탄소와 아주 밀접한 관계를 갖는다. 즉, 환경의 산화-환원 상태에 따라, 이산화탄소로부터 메탄은 생성되고 또한 이산화탄소로 산화돼 제거된다. 일반적으로 메탄은 유기물 분해(속성)과정 가장 마지막에 생성된다. 따라서, 메탄은 산소가 풍부한 수층보다는 무산소 퇴적층에서 주로 발생하고, 유기물이 많은 연안에서 대양보다 훨씬 많이 발생한다. 유기물 분해로 발생하는 메탄이 일반적이지만, 깊은 퇴적층에서 메탄은 다탄화수소(> C1)의 열성 변환으로 인해 생성되기도 한다. 대양 해저면과 극지방에서 발생하는 메탄은 낮은 온도 및 높은 압력으로 인해, 고체 형태인 하이드레이트(hydrate)로 저장되기도 한다. 퇴적층에서 발생하는 메탄은 확산, 이류(advection), 방울 형태로 수층 혹은 대기로 유출된다. 하지만, 대부분의 메탄은 황화물 환원 지역에서 산화되고, 이후 다른 터미널 전자 수용체(Fe/Mn(oxy)hydroxides, Nitrate, 등)에 의해 실제 수층으로 유입되는 메탄의 비율은 아주 낮다. 하지만, 퇴적층 메탄은 대부분 µM~mM 수준으로 있기 때문에 유출비율이 적다고 하더라도, 실제 농도는 해수 농도보다 훨씬 높다. 이후, 저층수로 유입된 메탄은 산소가 풍부한 수층에서 대부분 산화되어, 실제 대기로 유출되는 양은 초기 양보다 아주 적다(물론, 수심 및 파도 등, 물리-지질적 구조에 따라 유출량은 아주 큰 차이가 있다). 담수환경에서 메탄의 생지화학적 거동은 해상환경과 비슷하게 나타난다. 하지만, 일반적으로 담수에서 황화물 농도는 해수에 비해 아주 낮기 때문에, 황화물 환원에 의한 메탄 산화가 아주 낮다. 에 따라, 담수(육상)에서 메탄 유출량이 해양보다 월등히 높다. 종합하면, 메탄의 생지화학적 과정은 산소 농도에 따라 크게 영향을 받는다. 따라서, 저층수 저(빈)산소 환경은(특히 해양), 메탄 발생지역을 수층까지 넓힘과 동시에, 주요한 산화 지역인 황화물-메탄 전환(SMTZ) 구역을 퇴적층 상부로 이동시켜, 메탄의 수층 및 대기 유출을 좀 더 용이하게 할 것으로 여겨진다.
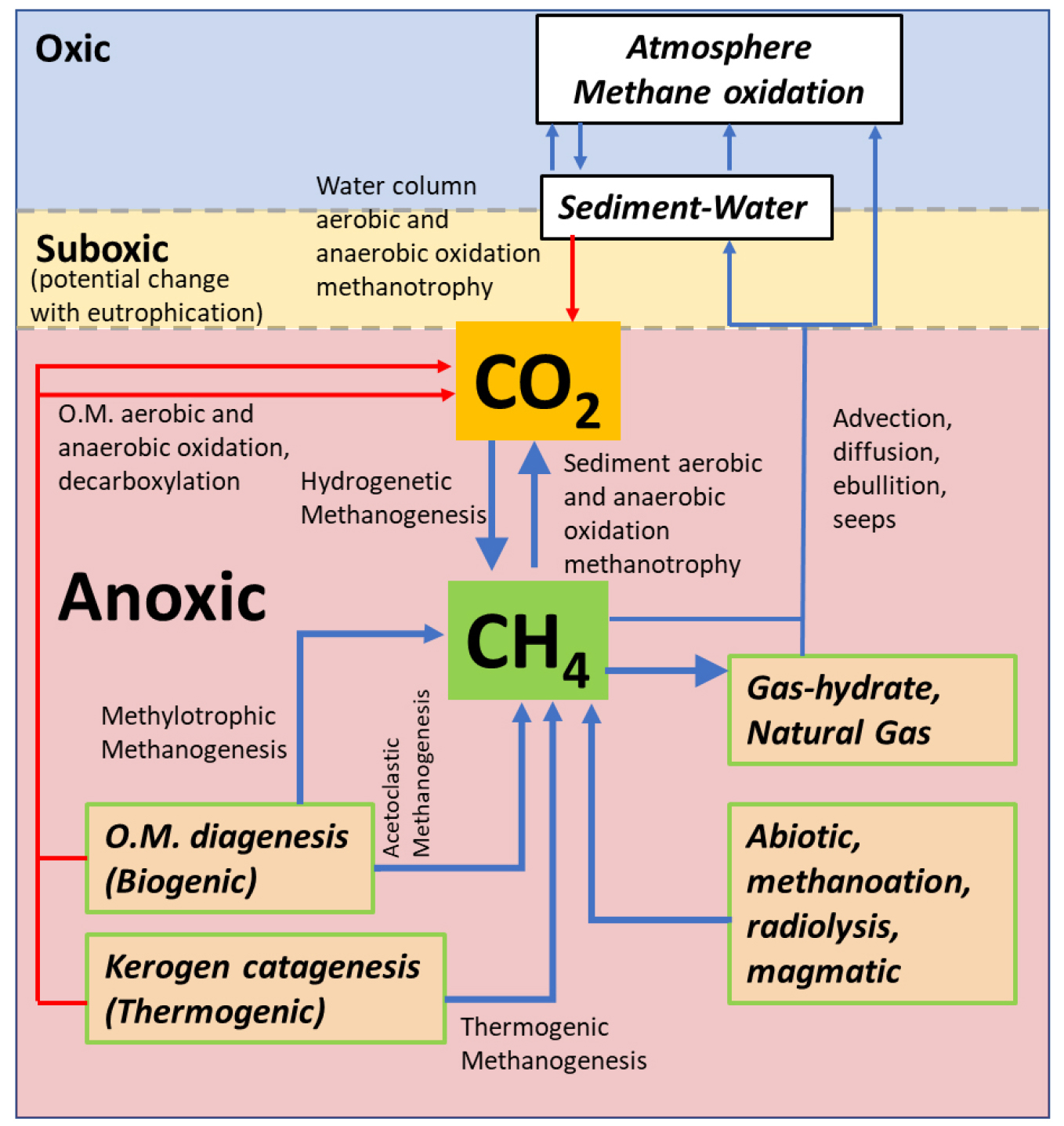
Fig. 7.
A simplified diagram of the methane production (blue arrow) and removal (red arrow) in the oxic- and anoxic conditions. This figure was modified from Whiticar(2020).
5. 결 론
최근 IPCC 보고서에서 미래 기후는 예상보다 빠르게 지구 온난화가 진행될 것으로 예측하였다. 이에 따라, 해양 및 빙권(cryosphere)에 저장된 온실기체의 유출이 더욱 가속화될 것으로 전망된다. 또한, 해양의 온도 증가는 물에 녹아 있는 기체의 대기 유출(degassing)을 야기하고, 또한 용해도가 낮아져 결과적으로 용존 산소를 비롯한 기체의 농도를 낮춘다. 또한, 육상으로부터 과도한 영양염 유입으로 연안 해역의 부영양화가 더욱 가속화되고, 이와 더불어 해수 온도 상승에 따른 물리적 특징 변화 등, 복합적 원인으로 해양 저산소층은 그 발생 지역과 유지 기간이 전 지구적으로 더욱 늘어날 전망이다. 해양 저산소층은 퇴적층에 분포해 있는 산화-환원 대(zone)를 보다 수층에 가깝게 형성되게 함으로써, 메탄 등의 온실기체가 해수 및 대기로 유출될 가능성을 높인다. 실제 세계 몇몇 지역에서는 해수 저산소층 발달 시기에 메탄 대기 유출량이 증가한 것으로 보고 되고 있다. 하지만, 전 세계적으로 저산소층-메탄 유출에 관한 연구가 미미한 수준이다. 특히, 한국은 강과 연안 해역 등 계절적 저산소층이 발생하는 곳이 점차 증가 추세여서, 이런 지역 내 온실기체(메탄, 아산화질소) 연구는 국내뿐만 아니라 국제적으로도 아주 중요한 지표가 될 것으로 생각된다. 이뿐만 아니라, 한국은 세계적으로 넓은 갯벌 등 온실기체가 배출될 수 있는 여러 환경이 존재하지만, 이에 관한 메탄(혹은 아산화질소와 같은 온실기체) 연구는 아직 많이 부족한 실정이다. 따라서, 본 리뷰 논문이, 이러한 연구 환경에 보다 많은 관심을 갖게 하는 계기가 되기를 기대한다.